AMFLEE 134 MG SOLUTION POUR SPOT-ON POUR CHIENS
2. Composition qualitative et quantitative
Une pipette de 1,34 mL contient :
Substance(s) active(s) :
Fipronil ……………………………………..……….. | 134,00 mg |
Excipient(s) :
Butylhydroxyanisole (E320) ……………...……….. | 0,27 mg |
Butylhydroxytoluène (E321) ………………..…….. | 0,13 mg |
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
3. Forme pharmaceutique
Solution pour spot on.
Liquide limpide jaune à jaune clair.
4. Informations cliniques
4.1. Espèces cibles
Chiens.
4.2. Indications d'utilisation, en spécifiant les espèces cibles
Chez les chiens :
- Traitement des infestations par les puces (Ctenocephalides spp.) et les tiques (Dermacentor reticulatus).
- Traitement des infestations par les poux broyeurs Trichodectes canis. La plupart des poux sont tués dans les deux jours.
Le produit a une durée de protection contre les nouvelles infestations par les puces adultes jusqu’à 8 semaines. L’efficacité acaricide persiste jusqu’à 3 semaines contre les tiques Ixodes ricinus et jusqu’à 4 semaines contre Rhipicephalus sanguineus et Dermacentor reticulatus. Si des tiques de certaines espèces (Ixodes ricinus, Rhipicephalus sanguineus) sont présentes au moment de l’application du produit, elles peuvent ne pas être toutes tuées dans les premières 48 heures.
Le médicament peut être intégré dans un programme thérapeutique de la Dermite Allergique par Piqûres de Puces (DAPP), quand celle-ci a été préalablement diagnostiquée par le vétérinaire.
4.3. Contre-indications
En l’absence de données disponibles, ne pas traiter les chiots de moins de 2 mois et/ou pesant moins de 2 kg.
Ne pas utiliser chez les animaux malades (maladies systémiques, fièvre...) ou convalescents.
Ne pas utiliser chez les lapins car des effets indésirables parfois létaux peuvent se produire.
Ce produit a été spécialement développé pour les chiens. Ne pas utiliser chez les chats car cela peut conduire à un surdosage.
Ne pas utiliser en cas d’hypersensibilité à la substance active, au diméthylsulfoxyde ou à l’un des autres excipients.
4.4. Mises en garde particulières à chaque espèce cible
Eviter tout bain/immersion dans l’eau dans les deux jours suivant l’application du produit. Après une immersion hebdomadaire dans l’eau pendant une minute, le produit a montré une rémanence de l’efficacité insecticide contre les puces de 7 semaines.
Le produit n'empêche pas les tiques de s'accrocher aux animaux. Si l'animal a été traité avant qu'il ne soit exposé aux tiques, celles-ci seront tuées dans les premières 24-48 heures après qu'elles se soient accrochées. Dans la plupart des cas, elles seront mortes avant qu'elles ne se soient gorgées de sang, ce qui minimise mais n'exclut pas la transmission des maladies. Une fois que les tiques sont mortes, elles tomberont de l'animal ; celles qui restent accrochées peuvent être enlevées en tirant doucement dessus.
Les puces des animaux domestiques infestent souvent leur panier, leur lieu de couchage ou leurs zones de repos telles que les tapis et les canapés. En cas d’infestation massive, au début du traitement, ces endroits doivent être traités, avec un insecticide adapté et aspirés régulièrement.
Dans le cadre d'un programme thérapeutique de traitement de la Dermite Allergique aux Piqûres de Puces (DAPP), il est recommandé de procéder à des applications mensuelles du produit sur l'animal hypersensible et de traiter les autres chiens et chats du foyer avec un insecticide approprié.
Pour un contrôle optimal de l’infestation par les puces dans un foyer contenant plusieurs animaux de compagnie, tous les animaux du foyer (i.e. chiens, chats, furets, lapins) doivent être traités avec un insecticide approprié.
4.5. Précautions particulières d'emploi
i) Précautions particulières d'emploi chez l'animal
Peser les animaux avec précision avant le traitement.
Eviter tout contact avec les yeux de l’animal. En cas de contact accidentel avec les yeux, rincer immédiatement et abondamment les yeux avec de l’eau.
Il est important de s’assurer que le produit est appliqué sur une zone que l’animal ne peut pas lécher et de s’assurer que les animaux ne se lèchent pas entre eux après le traitement.
Ne pas appliquer sur des plaies ou sur une peau abîmée.
ii) Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Ce produit peut occasionner une irritation des muqueuses et des yeux. Pour cette raison, éviter tout contact du produit avec la bouche et les yeux.
En cas de contact accidentel avec les yeux, les rincer immédiatement et abondamment à l’eau. Si l’irritation oculaire persiste, consulter un médecin et lui montrer la notice.
Ne pas fumer, boire ou manger pendant l’application.
Eviter de toucher le contenu de la pipette avec les doigts. Si cela se produit, se laver immédiatement les mains avec du savon et de l’eau.
Se laver les mains après utilisation.
Les personnes présentant une hypersensibilité connue au fipronil ou au diméthylsulfoxyde ou à l’un des excipients doivent éviter tout contact avec le médicament vétérinaire.
Tant que le site d’application n’est pas sec, les animaux traités ne doivent pas être manipulés et les enfants ne doivent pas être autorisés à jouer avec les animaux traités. Il est donc recommandé de ne pas traiter les animaux pendant la journée, mais en début de soirée et de ne pas laisser les animaux récemment traités dormir avec leurs propriétaires, surtout avec les enfants.
Conserver les pipettes dans le conditionnement extérieur d'origine et jeter immédiatement les pipettes utilisées.
iii) Autres précautions
Le fipronil peut nuire aux organismes aquatiques. Ne pas laisser les chiens se baigner dans des cours d’eau pendant les deux jours qui suivent le traitement.
4.6. Effets indésirables (fréquence et gravité)
Si l’animal se lèche, un bref épisode d’hypersalivation peut être observé.
Dans de très rares cas rares, des réactions cutanées transitoires au site d’application (squames, alopécie locale, prurit et érythème) et des cas de prurit ou alopécie généralisés ont été signalés. Des cas d’hypersalivation, des symptômes neurologiques réversibles (hyperesthésie, dépression, symptômes nerveux), des vomissements ou des symptômes respiratoires ont été observés dans de très rares cas après utilisation du médicament.
La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
4.7. Utilisation en cas de gestation, de lactation ou de ponte
Les études de laboratoire sur le fipronil n’ont pas mis en évidence d’effets tératogènes ou embryotoxiques. L’innocuité du produit n’a pas été établie chez les femelles reproductrices, ni en cas de gestation ou de lactation. L’utilisation du produit en cas de gestation ou de lactation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
4.8. Interactions médicamenteuses et autres formes d'interactions
Aucune connue.
4.9. Posologie et voie d'administration
Posologie et voie d'administration :
Usage externe uniquement.
Appliquer directement sur la peau en fonction du poids de l’animal : 1 pipette de 1,34 mL par animal pour un poids de plus de 10 kg et jusqu’à 20 kg.
Mode d’administration :
Retirer la pipette de son enveloppe. Tenir la pipette droite, dévisser et retirer le capuchon. Prendre le capuchon, le retourner et le placer à l’envers sur le bout allongé de la pipette. Appuyer et appliquer une rotation sur le capuchon afin de briser le joint. Retirer le capuchon.
Ecarter les poils de l’animal entre les omoplates afin de rendre la peau visible. Appliquer l’embout de la pipette directement sur la peau de l’animal et presser la pipette plusieurs fois afin de la vider de son contenu. Vider le contenu sur la peau en deux points.
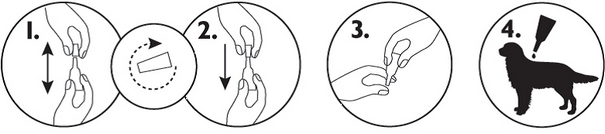
Il est important de s’assurer que le produit est appliqué à un endroit où l’animal ne peut se lécher et de vérifier que d’autres animaux ne peuvent lécher la zone de traitement.
Les poils doivent être écartés et le produit appliqué directement sur la peau. Des modifications de pelage (poil collant, gras ou présence de dépôts) peuvent être observées au site d’application.
Programme de traitement :
Afin d’assurer un contrôle optimal des infestations par les puces et les tiques, le programme de traitement doit être basé sur la situation épidémiologique locale.
En l’absence d’étude d’innocuité, l’intervalle de retraitement minimal est de 4 semaines.
4.10. Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Aucun effet secondaire n’a été observé dans les études d’innocuité menées sur des chiots de 8 semaines, des chiens en période de croissance et des chiens pesant environ 2 kg, traités une fois à 5 fois la dose recommandée. Cependant, le risque d’observer un effet secondaire (se reporter à la rubrique « Effets indésirables ») peut augmenter avec le surdosage, par conséquent les chiens doivent être traités avec la pipette correspondant au poids de l’animal.
4.11. Temps d'attente
Sans objet.
5. Propriétés pharmacologiques
Groupe pharmacothérapeutique : antiparasitaires externes pour usage topique.
Code ATC-vet : QP53AX15.
5.1. Propriétés pharmacodynamiques
Le fipronil est un insecticide acaricide, appartenant à la famille des phénylpyrazoles. Il agit en inhibant le complexe GABA, bloquant ainsi le transfert des ions chlore au travers de la membrane aux niveaux pré- et post-synaptiques en se fixant dans le canal chlore. Il provoque ainsi une activité incontrôlée du système nerveux central et la mort des insectes et des acariens.
Le fipronil présente une efficacité insecticide et acaricide sur les puces (Ctenocephalides spp), les tiques (Rhipicephalus spp, Dermacentor spp, Ixodes spp dont Ixodes ricinus, et les poux (Trichodectes canis) chez le chien. Les tiques sont généralement tuées dans les 48 heures après le contact avec le fipronil, si des tiques appartenant à certaines espèces (Ixodes ricinus, Rhipicephalus sanguineus) sont présentes au moment de l’application du produit, elles peuvent ne pas être toutes tuées dans les premières 48 heures. Les puces sont tuées en 24 heures.
5.2. Caractéristiques pharmacocinétiques
Le fipronil est principalement métabolisé en son dérivé sulfone (RM1602), qui possède aussi des activités insecticide et acaricide. Les concentrations de fipronil sur le poil diminuent avec le temps.
6. Informations pharmaceutiques
6.1. Liste des excipients
Butylhydroxyanisole (E320)
Butylhydroxytoluène (E321)
Polysorbate 80
Povidone K25
Diméthylsulfoxyde
6.2. Incompatibilités majeures
Aucune connue.
6.3. Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente: 3 ans.
6.4. Précautions particulières de conservation
Conserver dans le conditionnement d’origine afin de protéger le produit de la lumière et de l’humidité. Ne pas retirer du sachet jusqu’à utilisation.
Le produit doit être maintenu à température ambiante (au-dessus de 14°C) pendant environ une heure avant l'administration.
6.5. Nature et composition du conditionnement primaire
Pipette polypropylène
Bouchon polypropylène ou polyoxyméthylène
6.6. Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
Le fipronil peut nuire aux organismes aquatiques. Ne pas jeter le produit ou les emballages vide dans les étangs, les rivières et les ruisseaux.
7. Titulaire de l'autorisation de mise sur le marché
KRKA
SMARJESKA CESTA 6
8501 NOVO MESTO
SLOVENIE
8. Numéro(s) d'autorisation de mise sur le marché
FR/V/8306327 9/2015
Boîte de 1 sachet de 1 pipette de 1,34 mL
Boîte de 3 sachets de 1 pipette de 1,34 mL
Boîte de 6 sachets de 1 pipette de 1,34 mL
Boîte de 10 sachets de 1 pipette de 1,34 mL
Boîte de 20 sachets de 1 pipette de 1,34 mL
Boîte de 30 sachets de 1 pipette de 1,34 mL
Toutes les présentations peuvent ne pas être commercialisées.
9. Date de première autorisation/renouvellement de l'autorisation
25/02/2015 - 24/12/2019
10. Date de mise à jour du texte
04/03/2020