CYDECTINE LA 20 MG/ML SOLUTION INJECTABLE POUR OVINS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un mL contient : |
|
Substance(s) active(s) : |
|
Moxidectine | 20 mg |
Excipient(s) :
Composition qualitative en excipients et autres composants | Composition quantitative si cette information est essentielle à une bonne administration du médicament vétérinaire |
Alcool benzylique (E1519) | 70,0 mg |
Oléate de sorbitan | / |
Dicaprylocaprate de propylèneglycol | / |
Solution injectable jaune clair.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Ovins (à partir de 15 kg de poids vif).
3.2 Indications d'utilisation pour chaque espèce cible
Traitement et prévention des infestations mixtes par les nématodes gastro-intestinaux, les nématodes respiratoires et certains parasites arthropodes.
La moxidectine est indiquée pour le traitement des infestations provoquées par les souches sensibles à la moxidectine de :
- Nématodes gastro-intestinaux :
. Haemonchus contortus (adultes et L3)
. Ostertagia (Teladorsagia) circumcincta (adultes et L3, y compris les larves inhibées)
. Trichostrongylus axei (adultes)
. Trichostrongylus colubriformis (adultes et L3)
. Nematodirus spathiger (adultes)
. Cooperia curticei (macmasteri) (adultes)
. Cooperia punctata (adultes)
. Oesophagostomum columbianum (L3)
. Chabertia ovina (adultes)
- Nématodes de l'appareil respiratoire :
. Dictyocaulus filaria (adultes)
- Larves de diptères :
. Oestrus ovis (L1, L2, L3)
- Agents de la gale :
. Psoroptes ovis
Le médicament a une action rémanente et protège les moutons contre l'infestation ou la ré-infestation par les parasites suivants pendant la période indiquée :
Espèces | Période de protection (jours) |
Ostertagia (Teladorsagia) circumcincta | 97 |
Haemonchus contortus | 111 |
Trichostrongylus colubriformis | 44 |
Psoroptes ovis | 60 |
Les durées d'action rémanente n'ont pas été établies pour les espèces de parasites autres que celles incluses dans la liste ci-dessus. En conséquence, la ré-infestation des animaux sur des pâtures contaminées par des parasites autres que ceux-ci reste possible avant les 44 jours minimum de période de rémanence démontrée pour ces espèces spécifiques.
3.3 Contre-indications
Ne pas utiliser chez des moutons de moins de 15 kg de poids vif.
Ne pas injecter le produit par voie intravasculaire. L’injection intravasculaire peut entrainer ataxie, paralysie, convulsions, collapsus et la mort. Voir rubrique « Précautions particulières pour une utilisation sûre chez les espèces cibles ».
Ne pas utiliser dans les cas d'hypersensibilité à la substance active ou à l'un des excipients.
3.4 Mises en garde particulières
Une utilisation non justifiée d’antiparasitaires ou s'écartant des instructions du RCP peut augmenter la pression de sélection de la résistance et conduire à une efficacité réduite. La décision d'utiliser le produit doit être basée sur la confirmation de l'espèce et de la charge parasitaires, ou du risque d'infestation sur la base de ses caractéristiques épidémiologiques, pour chaque troupeau.
Veiller à éviter les pratiques suivantes, car elles augmentent le risque de développement de résistances et peuvent être la cause de l'inefficacité d'un traitement :
- Utilisation trop fréquente et répétée des anthelminthiques de la même classe sur une période prolongée.
- Sous-dosage qui peut être dû à une sous-estimation du poids vif, à une mauvaise administration du produit, ou à une absence de calibrage du dispositif d'administration (le cas échéant).
Les cas cliniques avec une suspicion de résistance aux anthelminthiques doivent être étudiés de manière approfondie en utilisant des tests appropriés (par exemple le test de réduction du nombre d'œufs dans les fèces). Lorsque les résultats du ou des tests suggèrent fortement une résistance à un anthelminthique particulier, un anthelminthique appartenant à une autre classe pharmacologique et ayant un mode d'action différent doit être utilisé.
La résistance aux lactones macrocycliques a été signalée pour Teladorsagia chez les moutons dans un certain nombre de pays. En 2008, dans toute l'Europe, la résistance à la moxidectine est très rare ; elle a été rapportée dans un seul cas concernant une souche de Teladorsagia circumcincta résistante au lévamisole, au benzimidazole et à l'ivermectine. Par conséquent, l'utilisation de la moxidectine doit être basée sur des informations épidémiologiques locales (régionale, élevage) sur la sensibilité des nématodes, l'historique local des traitements et les recommandations sur la manière d'utiliser le médicament dans des conditions durables pour limiter une sélection supplémentaire de la résistance aux anthelminthiques. Ces précautions sont particulièrement importantes lorsqu'on utilise la moxidectine pour contrôler des souches résistantes.
Des essais ont montré que la moxidectine était efficace contre certaines souches des espèces Haemonchus contortus, Teladorsagia circumcincta et Trichostrongylus spp. résistantes aux benzimidazoles.
Psoroptes ovis est un parasite externe extrêmement contagieux chez les ovins. Pour assurer un contrôle complet, il faut éviter la ré-infestation, puisque les agents de la gale peuvent survivre jusqu’à 15 jours hors de l’animal. Il est important de s'assurer que tous les ovins ayant été en contact avec des ovins infectés soient traités. Il est nécessaire d'éviter tout contact entre les troupeaux traités, infestés et non traités pendant au moins 7 jours après le traitement.
Une résistance à la moxidectine a été signalée chez les acariens de la gale Psoroptes ovis, chez les ovins et les bovins. Des cas de co-résistance avec d'autres lactones macrocycliques (ivermectine et doramectine) ont également été signalés. L'utilisation de ce produit doit tenir compte des informations locales sur la sensibilité des parasites cibles, lorsqu'elles sont disponibles.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Ce médicament a été formulé spécifiquement pour l'injection sous-cutanée à la base de l'oreille du mouton et ne doit pas être administré ni par une autre voie d'administration, ni à une autre espèce.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Eviter tout contact direct avec la peau ou les yeux.
Se laver les mains après utilisation.
Ne pas fumer, boire ou manger pendant la manipulation du médicament.
Eviter l'auto-injection. Si toutefois cela arrivait, il est peu vraisemblable que de quelconques symptômes associés au médicament soient observés. En cas d'auto-injection accidentelle, consulter immédiatement un médecin et lui montrer la notice ou l'étiquette. Conseil aux médecins en cas d'auto-injection accidentelle : traitement symptomatique.
Précautions particulières concernant la protection de l'environnement
La moxidectine remplit les critères pour être classée comme substance (très) persistante, bioaccumulable et toxique (PBT), par conséquent, l’exposition de l’environnement à la moxidectine doit être limitée autant que possible. Les traitements ne doivent être administrés que lorsque cela est nécessaire et doivent être basés sur le nombre d'œufs présents dans les excréments ou l’évaluation du risque d’infestation au niveau de l’animal et/ou du groupe.
À l’instar des autres lactones macrocycliques, la moxidectine peut entraîner des effets indésirables pour les organismes non ciblés :
- Les excréments contenant de la moxidectine excrétés dans les prairies par des animaux traités peuvent temporairement réduire l’abondance d’organismes se nourrissant de fumier. Après que des moutons ont été traités par le produit, des niveaux de moxidectine, potentiellement toxiques pour les espèces de mouches du fumier, peuvent être excrétés durant une période de plus de quatre semaines et peuvent réduire l’abondance de mouches du fumier durant cette période. Il a été établi lors d’essais en laboratoire que la moxidectine pouvait affecter temporairement la reproduction des coléoptères coprophages; toutefois, des études sur les résidus retrouvés n’ont indiqué aucun effet sur le long terme. Néanmoins, en cas de traitements répétés avec la moxidectine (tout comme avec les produits de la même classe des anthelminthiques), il est conseillé de ne pas traiter à chaque fois les animaux dans la même prairie afin de permettre aux populations de faune du fumier de se rétablir.
- La moxidectine est intrinsèquement toxique pour les organismes aquatiques, y compris les poissons. Le produit doit uniquement être utilisé conformément aux instructions de l’étiquetage. D’après le profil d’excrétion de la moxidectine lorsqu’elle est administrée sous forme de formulation injectable à des moutons, les animaux traités ne doivent pas pouvoir accéder aux cours d’eau durant les 11 premiers jours suivant le traitement.
Autres précautions
3.6 Effets indésirables
Ovins :
Très fréquent ( > 1 animal / 10 animaux traités) : | Gonflement au point d’injection1 Inflammation au site d’injection |
Rare (1 à 10 animaux / 10 000 animaux traités) : | Augmentation de la salivation2 Ataxie2, Somnolence2 Dépression2 |
Très rare ( < 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Troubles neurologiques3 (tels que collapsus, convulsions, paralysie) |
1 disparaît généralement sans traitement dans les 7 jours
2 transitoire, aucun antidote spécifique, aucun traitement particulier n'est nécessaire : ces symptômes disparaissent habituellement en 24 à 48 heures
3 réactions graves pouvant être mortelles
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir également la rubrique « Coordonnées » de la notice.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation :
Peut être utilisé pendant la gestation. Néanmoins, voir rubrique 3.3 « Contre-indications ».
3.8 Interactions médicamenteuses et autres formes d'interactions
Les effets des GABA agonistes sont augmentés par la moxidectine.
3.9 Voies d'administration et posologie
Voie sous-cutanée.
La dose est de 0,5 mL/10 kg de poids vif soit 1 mg de moxidectine par kg de poids vif. Les bouchons des flacons de 50 mL ne doivent pas être percés plus de 10 fois. Utiliser un dispositif de seringue automatique pour les présentations de 200 mL et 500 mL.
Un sous-dosage pourrait entraîner une utilisation inefficace et favoriser le développement de résistances. Pour permettre l'administration d'une dose correcte, le poids vif doit être déterminé le plus précisément possible ; la précision du dispositif d'administration doit être vérifiée. Si les animaux doivent être traités collectivement plutôt qu'individuellement, il faut les regrouper en fonction de leur poids vif et leur administrer le médicament en conséquence, afin d'éviter tout sous- ou surdosage.
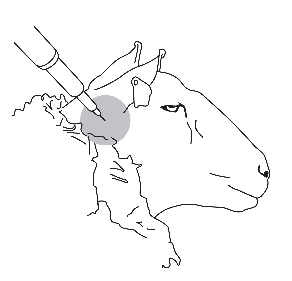
Le produit doit être administré par injection sous-cutanée unique à la base de l'oreille en utilisant une aiguille hypodermique de 25 mm de calibre 18. En maintenant la tête de l'animal, la formulation doit être administrée à la base de l'oreille à environ 2 cm en arrière du bord antérieur du pavillon. La peau à la base de l'oreille choisie doit être pincée et le médicament injecté dans le tissu sous-cutané. Après l'administration sous-cutanée, l'aiguille doit être retirée de la peau en appliquant une pression avec le pouce au point d'injection pendant plusieurs secondes. Si une fuite se produit, il faut alors appliquer la pression pendant quelques secondes de plus.
Diagramme : procédure d'injection auriculaire
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Des signes de surdosage n'ont pas été observés à 3 et 5 fois la dose recommandée. Toutefois, s'ils apparaissent, ils devraient correspondre au mode d'action de la moxidectine et se manifester par une salivation, une dépression, une somnolence et une ataxie transitoires, 24 à 36 heures après le traitement. Les signes disparaissent habituellement dans les 36 à 72 heures sans traitement. Il n'existe pas d'antidote spécifique.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Viande et abats : 104 jours.
Lait : interdit chez les brebis laitières, à tous les stades de leur vie.
Le temps d'attente est calculé après injection unique à la base de l'oreille.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QP54AB02
4.2 Propriétés pharmacodynamiques
La moxidectine est un endectocide actif contre un large spectre de parasites internes et externes. C'est une lactone macrocyclique de seconde génération de la famille des milbémycines.
La moxidectine interagit avec les récepteurs GABA et les canaux chlore. L'effet net est l'ouverture des canaux chlore sur la jonction post-synaptique pour permettre l'afflux d'ions chlore et induire un état de repos irréversible. Ceci entraîne une paralysie flasque et finalement la mort des parasites exposés au médicament.
Le produit a une activité rémanente sur les seconds stades larvaires d’Oestrus ovis (larves L2 seulement) jusqu'à 80 jours après traitement.
Cependant, il n'y a pas de prévention de la réinfestation avec les larves de 1er stade et on peut observer pendant cette période des signes cliniques liés à cette réinfestation.
La résistance à la moxidectine est médiée en partie par les transporteurs membranaires P-glycoprotéines, et une résistance croisée avec d'autres lactones macrocycliques est possible.
4.3 Propriétés pharmacocinétiques
La moxidectine est absorbée après injection sous-cutanée et les concentrations sanguines maximales (Cmax 24 ng/mL) sont atteintes 4 à 7 jours après l'injection. L'AUC moyenne est de 411 ng.j/mL. Le médicament est distribué dans tous les tissus de l'organisme mais, du fait de sa lipophilie, est concentré essentiellement dans le tissu adipeux. La demi-vie d'élimination dans la graisse est de 30 à 34 jours.
La moxidectine subit une biotransformation par hydroxylation dans le corps. Les fèces constituent l'unique voie d'excrétion significative.
Propriétés environnementales
La moxidectine remplit les critères pour être qualifiée de substance (très) persistante, bioaccumulable et toxique (PBT). Plus particulièrement, dans des études sur la toxicité aiguë et chronique sur des algues, des crustacés et des poissons, la moxidectine a montré une toxicité pour ces organismes, donnant lieu aux résultats suivants:
Organisme | CE50 | CSEO | |
Algues | S.capricornutum | > 86,9 µg/L | 86,9 µg/L |
Crustacés (puces d’eau) | Daphniamagna (aiguë) | 0,0302 µg/L | 0,011 µg/L |
Daphniamagna (reproduction) | 0,0031 µg/L | 0,010 µg/L | |
Poissons | O.mykiss | 0,160 µg/L | Indéterminée |
L.macrochirus | 0,620 µg/L | 0,52 µg/L | |
P.promelas (premiers stades de la vie) | Sans objet | 0,0032 µg/L | |
| Cyprinuscarpio | 0,11 µg/L | Indéterminée |
CE50: concentration qui entraîne des effets indésirables chez 50 % des animaux d’une espèce testée, à savoir la mortalité et les effets sublétaux.
CSEO: dans l’étude, concentration à laquelle aucun effet n’est observé.
Cela signifie que lorsque la moxidectine pénètre dans des organismes aquatiques, cela peut avoir une incidence grave et durable sur la vie aquatique. Afin d’atténuer ce risque, toutes les précautions d’emploi et d’élimination doivent être respectées.
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
En l'absence d'études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé à d'autres médicaments vétérinaires.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
Durée de conservation après première ouverture du conditionnement primaire : 28 jours.
5.3 Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
Conserver le flacon dans l’emballage extérieur de façon à le protéger de la lumière.
5.4 Nature et composition du conditionnement primaire
Flacons polyéthylène haute densité naturel avec bouchons caoutchouc chlorobutyle revêtus de Flurotec et capsule flip-off aluminium (50 mL) ou capsule aluminium (200 mL, 500mL).
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Le médicament vétérinaire ne doit pas être déversé dans les cours d’eau car la moxidectine pourrait mettre les poissons et autres organismes aquatiques en danger.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
ZOETIS FRANCE
10 RUE RAYMOND DAVID
92240 MALAKOFF
FRANCE
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/7672854 5/2008
Boîte de 1 flacon de 50 mL
Boîte de 1 flacon de 200 mL
Boîte de 1 flacon de 500 mL
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
08/12/2008 - 20/11/2013
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
08/04/2024
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).