DECTOSPOT 10 MG/ML SOLUTION POUR-ON POUR BOVINS ET OVINS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un mL contient : |
|
|
|
Substance(s) active(s) : |
|
Deltaméthrine | 10 mg |
Excipient(s) :
Composition qualitative en excipients et autres composants |
Triglycérides à chaîne moyenne |
Liquide huileux limpide de couleur or pâle.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Bovins et ovins.
3.2 Indications d'utilisation pour chaque espèce cible
Chez les bovins : traitement et prévention des infestations par les poux piqueurs et broyeurs, incluant Bovicola bovis, Solenopotes capillatus, Linognathus vituli et Haematopinus eurysternus. Également indiqué comme aide au traitement et en prévention des infestations par les mouches piqueuses ou par les mouches lécheuses, incluant Haematobia irritans, Stomoxys calcitrans, Musca spp. et Hydrotaea irritans.
Chez les ovins : traitement et prévention des infestations par les tiques Ixodes ricinus, par les poux (Linognathus ovillus, Bovicola ovis) et par les mélophages (Melophagus ovinus) et traitement des cas établis de myiases cutanées (généralement causés par Lucilia spp.).
Chez les agneaux : traitement et prévention des infestations par les tiques Ixodes ricinus et par les poux Bovicola ovis.
3.3 Contre-indications
Ne pas utiliser chez des animaux convalescents ou malades.
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
Une utilisation hors AMM du médicament vétérinaire chez les espèces non cibles, telles que les chiens et les chats, peut entraîner des signes de toxicité neurologique (ataxie, convulsions, tremblements) et digestive (hypersalivation, vomissements), qui peut être fatale.
Ne pas utiliser chez des animaux présentant des lésions cutanées étendues.
3.4 Mises en garde particulières
Le médicament vétérinaire conduira à une réduction du nombre de mouches en contact direct avec les animaux, mais n’est pas censé éliminer toutes les mouches présentes dans la ferme. Des cas de résistance à la deltaméthrine ont été signalés. Toute utilisation stratégique du médicament vétérinaire devra donc reposer sur les informations épidémiologiques locales et régionales concernant la sensibilité des parasites et se fera en association avec d’autres méthodes de lutte antiparasitaire.
Veiller à éviter les pratiques suivantes, car elles augmentent le risque de développement d’une résistance qui pourrait à long terme rendre le traitement inefficace :
- utilisation trop fréquente et répétée d’antiparasitaires externes de la même classe sur une période prolongée ;
- sous-dosage pouvant être dû à une sous-estimation du poids corporel, à une mauvaise administration du médicament vétérinaire ou à l’absence d’étalonnage du dispositif d’administration.
Des cas de résistance à la deltaméthrine ont été signalés pour les mouches piqueuses et les mouches lécheuses chez les bovins et pour les poux chez les ovins.
L’utilisation inutile d’antiparasitaires ou une utilisation s’écartant des instructions données dans le résumé des caractéristiques du produit peut augmenter le développement d’une résistance qui pourrait à long terme rendre le traitement inefficace. Par conséquent, la décision d’utiliser le médicament vétérinaire doit être prise après confirmation de l’espèce et de la charge parasitaires, ou du risque d’infestation en fonction de ses caractéristiques épidémiologiques, pour chaque groupe d’animaux.
L’utilisation de ce produit nécessite la consultation des informations locales sur la sensibilité des parasites ciblés, le cas échéant.
Il est recommandé de poursuivre les recherches en cas de suspicion de résistance, avec une méthode de diagnostic appropriée.
La résistance confirmée doit être notifiée au titulaire de l’autorisation de mise sur le marché ou aux autorités compétentes.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Le médicament vétérinaire est destiné uniquement à un usage externe.
Ne pas appliquer dans les yeux et sur les muqueuses de l’animal, ou à proximité de ces zones, car la deltaméthrine est une substance irritante.
Veiller à éviter le léchage du médicament vétérinaire par les animaux. Éviter d’appliquer le médicament vétérinaire par forte chaleur et s’assurer que les animaux aient aisément accès à l’eau de boisson.
Le médicament vétérinaire doit être appliqué uniquement sur une peau saine, car il peut être toxique en cas d’absorption au niveau de lésions cutanées importantes. Toutefois, des signes d’irritation locale peuvent apparaître après le traitement si la peau a déjà été affectée par l’infestation.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Les personnes présentant une hypersensibilité connue à la substance active ou à l’un des excipients doivent éviter tout contact avec le médicament vétérinaire.
Un équipement de protection consistant en un tablier et des bottes imperméables et des gants étanches doit être porté lors de l’application du médicament vétérinaire ou de la manipulation d’animaux récemment traités.
Retirer immédiatement tout vêtement fortement contaminé et le laver avant de le porter à nouveau.
En cas de projection du produit, laver immédiatement la peau avec du savon et beaucoup d’eau.
Après avoir manipulé ce médicament vétérinaire, se laver les mains et laver toute zone de peau exposée.
En cas de contact avec les yeux, les rincer immédiatement et abondamment à l’eau courante propre et consulter un médecin.
En cas d’ingestion accidentelle, se rincer immédiatement la bouche à grande eau, consulter un médecin et lui montrer la notice ou l’étiquette.
Ne pas fumer, boire ou manger pendant la manipulation du médicament vétérinaire.
Ce produit contient de la deltaméthrine, qui peut causer des picotements, des démangeaisons et des éruptions rougeâtres sur la peau exposée. En cas de malaise après avoir manipulé ce médicament vétérinaire, demander immédiatement conseil à un médecin et lui montrer la notice ou l’étiquette.
Précautions particulières concernant la protection de l'environnement
La deltaméthrine est très toxique pour les bousiers, les organismes aquatiques et les abeilles mellifères. Elle persiste dans les sols et peut s’accumuler dans les sédiments.
Le risque pour les écosystèmes aquatiques et les bousiers peut être diminué en évitant un usage trop fréquent et répété de la deltaméthrine (et d’autres pyréthrinoïdes synthétiques) chez les bovins et les ovins, par exemple en appliquant un traitement par an seulement sur un même pâturage.
Le risque pour les écosystèmes aquatiques sera davantage réduit en maintenant les animaux traités à l’écart des cours d’eau dans l’heure qui suit le traitement.
Autres précautions
3.6 Effets indésirables
Bovins et ovins :
Très rare ( < 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Signes neurologiques (agitation1 ou prostration, tremblements, mouvements anormaux) Troubles cutanés (squamosis de la peau au point d’application, photosensibilisation, prurit)2 |
1 Générale
2 Observés dans les 48 heures suivant le traitement.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir également la rubrique « coordonnées » de la notice.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation et lactation :
L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation et de lactation.
Les études de laboratoire chez le rat et le lapin n’ont pas mis en évidence d’effets tératogènes.
L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
3.8 Interactions médicamenteuses et autres formes d'interactions
Ne pas utiliser avec d’autres insecticides ou acaricides.
La toxicité de la deltaméthrine est augmentée en association, en particulier, avec des composés organophosphorés.
3.9 Voies d'administration et posologie
Usage externe. Application en pour-on.
Un sous-dosage peut entraîner une utilisation inefficace et favoriser le développement d’une résistance.
Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible. Si les animaux doivent être traités en groupe, il faut former des groupes raisonnablement homogènes, et tous les animaux d’un groupe doivent recevoir la dose correspondant à l’animal le plus lourd.
Posologie :
Bovins : 100 mg de deltaméthrine par animal, soit 10 mL de médicament vétérinaire.
Ovins : 50 mg de deltaméthrine par animal, soit 5 mL de médicament vétérinaire.
Agneaux (de moins de 10 kg de poids vif ou âgé de moins d’un mois) : 25 mg de deltaméthrine par animal, soit 2,5 mL de médicament vétérinaire.
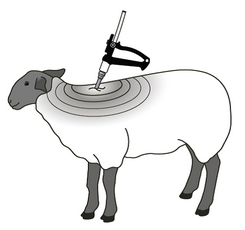
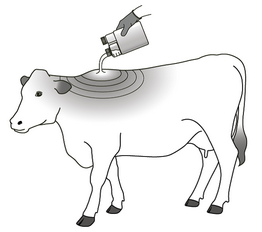
Appliquer le médicament vétérinaire non dilué en un seul point entre les épaules de l’animal comme illustré dans le schéma ci-dessous.
Pour le traitement et la prévention des infestations par les tiques, les mélophages et les poux chez les ovins, écarter les poils de la toison et appliquer le produit sur la peau de l’animal. Pour que l’efficacité soit maximale, il est recommandé de respecter les consignes suivantes :
- traiter peu après la tonte (animaux à toison courte),
- maintenir les ovins traités à l’écart des ovins non traités pour éviter toute ré-infestation.
La protection contre les mouches est maintenue pendant 4 à 6 semaines.
Poux chez les bovins : en règle générale, une application éradiquera tous les poux. L’éradication complète peut prendre 4 à 5 semaines, période pendant laquelle les œufs éclosent et les poux sont tués. Quelques poux peuvent survivre sur une petite minorité d’animaux.
Mélophages et poux chez les ovins : une application réduira l’incidence de l’infestation par les poux piqueurs ou les mélophages sur la période de 4 à 6 semaines qui suit le traitement.
Cas établis de myiases cutanées des ovins : appliquer directement sur la zone infestée de mouches dès que les myiases sont détectées. Une seule application permet de s’assurer que les larves de mouche sont tuées en peu de temps. En cas de lésions plus avancées dues à la myiase, il est conseillé de tondre la laine souillée avant le traitement.
L’influence des conditions météorologiques sur la durée de l’efficacité du traitement n’a pas été étudiée.
La durée de la période de prévention contre Musca spp. peut varier.
Le médicament doit être appliqué à l’aide d’un dispositif approprié :
- Pour les présentations de 250 mL et de 500 mL, utiliser une chambre graduée raccordée au flacon.
- Pour les présentations de 1 litre et de 2,5 litres, il est recommandé d’utiliser un applicateur approprié.
Pour être approprié, l’applicateur doit être conforme aux spécifications suivantes :
- il doit délivrer des doses de 5 mL et de 10 mL.
- il doit être doté d’un tuyau flexible dont le diamètre interne est compris entre 6 mm et 12 mm.
La procédure d’utilisation des dispositifs d’application qui est recommandée est illustrée dans les schémas ci-dessous.
1. Utilisation de la chambre graduée sur les flacons de 250 mL et de 500 mL :
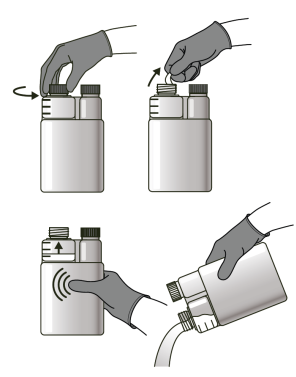
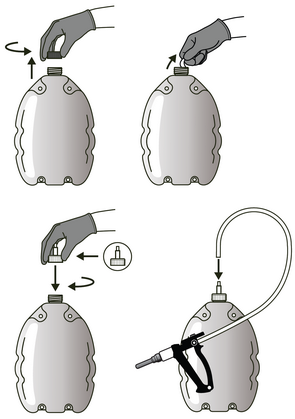
2. Raccordement des flacons de 1 et de 2,5 litres à un applicateur approprié :
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Certains effets indésirables ont été rapportés suite à un surdosage, dont des cas de paresthésie et d’irritation chez les bovins et de mictions intermittentes et tentatives de miction chez les jeunes agneaux. Ces effets légers et passagers rétrocèdent spontanément sans traitement.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet
3.12 Temps d'attente
Bovins :
Viande et abats : 18 jours
Lait : zéro heure
Ovins :
Viande et abats : 35 jours
Lait : 24 heures
La pratique du toilettage (léchage) est associée à un important risque de contamination croisée avec les animaux non traités avec ce médicament vétérinaire. Les animaux traités doivent donc être maintenus séparés sur une période qui correspond au temps d’attente maximum. Les animaux non traités pourraient présenter des résidus si cette recommandation n’est pas respectée.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QP53AC11
4.2 Propriétés pharmacodynamiques
La deltaméthrine est une molécule de la famille des pyréthrinoïdes synthétiques caractérisée par son activité insecticide et acaricide. Elle agit en modifiant la perméabilité des canaux sodiques, induisant une hyperexcitation suivie par une paralysie (effet choc ou knock-down) associée à des tremblements et la mort des parasites. Deux mécanismes physiologiques sont susceptibles de contribuer à la résistance à la deltaméthrine : mutation de la cible moléculaire de deltaméthrine ou sélection génomique conduisant à une augmentation de l’expression des enzymes mitochondriales oxydases et estérases.
4.3 Propriétés pharmacocinétiques
Après une application cutanée, la deltaméthrine est légèrement absorbée à travers la peau des bovins et des ovins.
Les pyréthrinoïdes sont métabolisés par les voies oxydatives et neurotoxiques.
Chez les animaux cibles, l’excrétion de la quantité absorbée se fait principalement par voie fécale.
Propriétés environnementales
La deltaméthrine est susceptible d’avoir un effet nocif sur des organismes non cibles vivant dans l’eau et les bouses. Après le traitement, une excrétion de la deltaméthrine à des taux potentiellement toxiques peut avoir lieu sur une période de 4 semaines. Les matières fécales contenant de la deltaméthrine excrétées sur les pâturages par les animaux traités peuvent réduire les effectifs des organismes coprophages, ce qui peut avoir un impact sur la dégradation des bouses.
La deltaméthrine est très toxique pour les bousiers, les organismes aquatiques et les abeilles mellifères. Elle persiste dans les sols et peut s’accumuler dans les sédiments.
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Aucune connue.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
Durée de conservation après première ouverture du conditionnement primaire : 3 mois.
5.3 Précautions particulières de conservation
À conserver en position verticale dans le récipient d’origine.
Conserver le récipient dans l’emballage extérieur de façon à le protéger de la lumière.
À conserver à l’écart des aliments et boissons pour animaux.
5.4 Nature et composition du conditionnement primaire
Flexipacks de 250 mL et 500 mL en polyéthylène haute densité avec distributeur à double col, chambre d’étalonnage interne graduée et bouchon à vis thermoscellée en polypropylène.
Bidons de 1 litre et 2,5 litres à fond plat en polyéthylène haute densité avec bouchons inviolables en polypropylène et ouate thermoscellée par induction. Un bouchon à bec est fourni avec les présentations de 1 litre et de 2,5 litres.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Le médicament vétérinaire ne doit pas être déversé dans les cours d’eau car la deltaméthrine pourrait mettre les poissons et autres organismes aquatiques en danger.
Ne pas contaminer les étangs, les cours d’eau ou les fossés avec le produit ou les conditionnements vides.
Utiliser les dispositifs de reprise mise en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et a tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
BIMEDA ANIMAL HEALTH
UNIT 2/3/4 AIRTON CLOSE
TALLAGHT
DUBLIN 24 DUBLIN
IRLANDE
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/6739546 0/2016
Boîte de 1 flacon de 250 mL
Boîte de 1 flacon de 500 mL
Boîte de 1 bidon de 1 litre avec bouchon à bec
Boîte de 1 bidon de 2,5 litres avec bouchon à bec
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
04/02/2016 - 22/12/2020
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
21/12/2023
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).