DUOFLECT SOLUTION POUR SPOT-ON POUR CHIENS DE 40 - 60 KG
2. Composition qualitative et quantitative
Une pipette de 4,2 mL contient : |
|
|
|
Substance(s) active(s) : |
|
Fipronil.................................................................................................. | 721,00 mg |
(S)-méthoprène.......................................................................................... | 360,00 mg |
|
|
Excipient(s) : |
|
Butylhydroxyanisole (E320)................................................................... | 0,85 mg |
Butylhydroxytoluène (E321).................................................................. | 0,85 mg |
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
3. Forme pharmaceutique
Solution pour spot-on.
Solution jaunâtre.
4. Informations cliniques
4.1. Espèces cibles
Chiens de 40 - 60 kg.
4.2. Indications d'utilisation, en spécifiant les espèces cibles
Chez les chiens :
- Traitement et prévention des infestations par les puces et/ou les tiques.
-Traitement et prévention des infestations par les puces (Ctenocephalides spp.). L'efficacité insecticide immédiate prévient de toute nouvelle infestation par les puces adultes pendant 9 semaines. Prévention de la multiplication des puces par inhibition du développement des œufs (activité ovicide) et des larves issues des œufs pondus par les puces adultes, pendant 8 semaines après application.
- Traitement et prévention des infestations par les tiques (Dermacentor reticulatus, Rhipicephalus sanguineus). Le produit a une efficacité acaricide immédiate et persistante pendant 6 semaines après application.
Le médicament peut être intégré dans un programme de traitement de la Dermatite par Allergie aux Piqûres de Puces (DAPP), lorsque ce diagnostic a été posé par un vétérinaire.
4.3. Contre-indications
Ne pas utiliser chez les lapins car des effets indésirables parfois létaux pourraient survenir.
Ne pas utiliser en cas d'hypersensibilité à la substance active ou à l'un des excipients.
Ne pas utiliser chez les animaux malades (par exemple : maladies systémiques, fièvre) ou convalescents.
4.4. Mises en garde particulières à chaque espèce cible
La fixation de tiques isolées après le traitement reste possible. Par conséquent, la transmission de maladies infectieuses ne peut être totalement exclue si les conditions sont défavorables.
Tous les stades de développement des puces peuvent infester le panier du chien, son lieu de couchage et ses zones de repos régulières tels que les tapis et canapés. En cas d'infestation massive de puces et au début des mesures de contrôle, ces zones doivent être traitées avec un insecticide pour l'environemment approprié. Pour réduire la pression parasitaire, tous les animaux du foyer doivent être traités avec un insecticide approprié.
Pour le traitement et le contrôle de la dermatite allergique aux piqûres de puces, il est recommandé que les patients allergiques et tous les autres animaux de la maison soient traités sur une base régulière.
Des études sur les effets d'un bain sur l'efficacité du produit contre les puces ont été effectuées chez le chien.
Une immersion dans l'eau de façon hebdomadaire après le traitement n'affecte pas la durée de l'efficacité. L'utilisation d'un shampooing émollient 48 heures avant le traitement n'a eu aucun effet sur la durée de l'efficacité. Un shampooing hebdomadaire avec un shampooing émollient chez les chiens peut réduire la durée de l'efficacité à 3 semaines contre les puces adultes et 6 semaines contre les stades immatures de puces. Un bain hebdomadaire avec un shampooing à base de chlorhexidine peut réduire l'efficacité contre les puces adultes à 3 semaines.
4.5. Précautions particulières d'emploi
i) Précautions particulières d'emploi chez l'animal
Voie externe uniquement. Ne pas administrer par voie orale.
Eviter tout contact avec les yeux de l'animal. En cas de contact accidentel du médicament vétérinaire avec les yeux, laver immédiatement et abondamment à l'eau.
Ne pas appliquer le médicament vétérinaire sur des plaies ou des lésions cutanées.
Laisser sécher complètement le point d'application avant de permettre au chien traité d'entrer en contact avec du mobilier ou des tissus.
Il est important de s'assurer que le produit est appliqué sur une zone de peau sèche ou l'animal ne peut pas se lécher. Veiller à ce que les animaux qui viennent d'être traités ne se lèchent pas entre eux.
En l'absence de données d'innocuité complémentaires, ne pas répéter le traitement à intervalle de moins de 2 semaines.
L'innocuité du produit n'a pas été établie chez les chiots de moins de 8 semaines d'âge et pesant moins de 2 kg de poids corporel.
ii) Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Ce médicament vétérinaire peut provoquer une irritation des muqueuses, de la peau et des yeux.
Aussi, éviter tout contact du produit avec la bouche, les yeux ou la peau.
En cas de contact accidentel avec les yeux, rincer immédiatement et abondamment les yeux avec de l’eau. En cas d’irritation oculaire persistante, prendre un avis médical et montrez la notice ou l’étiquette au médecin.
Eviter de toucher le contenu de la pipette avec les doigts. Si cela se produit, se laver les mains avec du savon et de l'eau.
Les personnes présentant une hypersensibilité connue au fipronil et/ou au (S)-méthoprène ne doivent pas traiter leur animal.
Ce produit peut provoquer une neurotoxicité et être nocif en cas d'ingestion. Éviter d’ingérer le produit et éviter également le contact main - bouche.
Ne pas manipuler ou jouer avec les animaux pendant au moins 12 heures après le traitement. Il est donc recommandé de traiter les animaux dans la soirée afin de limiter le contact avec l'animal traité. Le jour du traitement, il est conseillé de ne pas laisser les animaux traités dormir avec leurs maîtres, en particulier les enfants.
Ne pas manger, boire ou fumer pendant l'application du médicament vétérinaire.
En cas d’ingestion accidentelle, prendre immédiatement un avis médical et montrez la notice au médecin.
Se laver les mains soigneusement après usage.
Conserver les pipettes dans l'emballage d'origine jusqu'au moment de les utiliser.
Jeter immédiatement les pipettes utilisées de manière appropriée afin d’éviter leur accès aux enfants.
iii) Autres précautions
Le fipronil et le (S)-méthoprène peuvent avoir des effets indésirables sur les organismes aquatiques. Ne pas laisser les chiens traités nager dans des cours d'eau pendant les 2 jours suivant l'application.
4.6. Effets indésirables (fréquence et gravité)
Des modifications esthétiques transitoires au point d’application telles qu'un aspect humide, des poils ébouriffés, des dépôts secs ou de légères squames ont été très rarement observés dans des rapports spontanés de pharmacovigilance. Ces modifications n'altèrent pas l'efficacité et l'innocuité du produit.
Une hypersalivation transitoire après léchage du produit a été très rarement observée dans des rapports spontanés de pharmacovigilance, elle est principalement liée à la nature de l'excipient. Après l'ingestion du produit, certains chiens peuvent également vomir. Chez le chien, des vomissements après ingestion du produit ont été très rarement observés dans des rapports spontanés de pharmacovigilance.
La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
4.7. Utilisation en cas de gestation, de lactation ou de ponte
Les études de laboratoire sur le fipronil n'ont pas mis en évidence d'effets tératogènes ou embryotoxiques, bien qu'une neurotoxicité ait été montrée chez le rat.
L’innocuité du produit n’a pas été établie chez les chiens pendant la gestation et l'allaitement. L’utilisation ne doit se faire qu'après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
4.8. Interactions médicamenteuses et autres formes d'interactions
Aucune connue.
4.9. Posologie et voie d'administration
Application en spot-on.
Chiens de 40-60 kg.
Une pipette par animal correspondant à une dose minimale recommandée de 12 mg/kg de poids corporel de fipronil et 6 mg/kg de poids corporel de (S)-méthoprène.
Le traitement peut être répété toutes les 6 semaines, ou bien être adapté selon le type et le niveau d'exposition parasitaire. En l'absence d'études, le traitement ne doit pas être répété à des intervalles de moins de 2 semaines.
Comment appliquer le produit :
Détacher l'une des alvéoles de la plaquette. Cela permet d'éviter l'ouverture accidentelle du reste de la plaquette qui protège les pipettes encore non entamées de l'humidité. Ouvrir l'alvéole avec des ciseaux. Pour ne pas endommager la pipette, couper en suivant la ligne marquée par une paire de ciseaux. Retirer délicatement la feuille aluminium à partir de l'extrémité découpée et sortir la pipette.
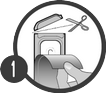
Tenir la pipette à la verticale. Tapoter légèrement la pipette pour faire descendre tout le contenu liquide dans le corps de la pipette. Rabattre la partie située au-dessus de la pipette vers l'arrière. La pipette peut maintenant être inclinée, si nécessaire. Pour ouvrir la pipette, rompre son embout en le pliant d'un coup sec au niveau du trait prédécoupé.
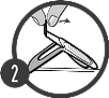
Ecarter les poils entre les omoplates de telle façon que la peau soit visible. Placer l'embout de la pipette sur la peau et presser la pipette à plusieurs reprises pour la vider entièrement de son contenu directement sur la peau et en un seul point.
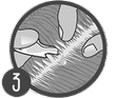
L'application de la solution à proximité de la base du cou permet de limiter le risque de léchage. Veiller à ce que les animaux ne se lèchent pas entre eux après le traitement.
On veillera à éviter de trop mouiller le pelage avec le produit, car il en résulterait un aspect de poils collants à l'endroit traité.
4.10. Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Aucun effet indésirable n'a été observé lors d'une étude de tolérance chez l'animal cible réalisée sur des chiots âgés de 8 semaines pesant environ 2 kg de poids corporel, traités 7 fois de suite à intervalles de 2 semaines avec jusqu'à 5 fois la dose recommandée.
4.11. Temps d'attente
Sans objet.
5. Propriétés pharmacologiques
Groupe pharmacothérapeutique : antiparasitaires externes pour usage cutanée, combinaisons de fipronil.
Code ATC-vet : QP53AX65.
La spécialité est une solution acaricide et insecticide pour usage topique, contenant en association un principe actif adulticide, le fipronil, et un principe actif ovicide et larvicide, le (S)-méthoprène.
5.1. Propriétés pharmacodynamiques
Le fipronil est un insecticide et un acaricide appartenant à la famille des phénylpyrazolés. Il agit en inhibant le système GABA, en se liant au canal chlore et en bloquant ainsi le passage pré- et post-synaptique des ions chlorures au travers de la membrane cellulaire. Il provoque ainsi une activité incontrôlée du système nerveux central des insectes et des acariens et leur mort. Le fipronil agit par contact. Après administration par voie topique, le fipronil s'accumule dans les glandes sébacées et est libéré progressivement sur la surface des poils par des conduits folliculaires. Le fipronil tue généralement les puces dans les 24 heures et les tiques dans les 48 heures.
Le (S)-méthoprène est un régulateur de la croissance des insectes (IGR) de la classe des analogues de l'hormone juvénile; il inhibe le développement des formes immatures des insectes. Mimant l'action de l'hormone juvénile, le composé provoque une altération du développement et la mort des formes immatures de puces. Le (S)-méthoprène agit par contact. L'activité ovicide du (S)-méthoprène appliqué sur l'animal résulte soit de sa pénétration directe dans la coquille des oeufs de puce qui viennent d'être pondus soit de son absorption à travers la cuticule des puces adultes. Le (S)-méthoprène est également efficace dans la prévention du développement des larves et pupes de puce, ce qui prévient la contamination de l'habitat des animaux traités par les stades immatures de puces.
5.2. Caractéristiques pharmacocinétiques
Fipronil
Le fipronil est faiblement absorbé par la peau. Après application topique dans des conditions cliniques (léchage non empêché), le pic de concentration plasmatique du fipronil (Cmax moyenne de 25,5 ng / mL) est lentement atteint (Tmax moyen d'environ 96 h). Le fipronil est métabolisé en fipronil sulfone.
(S)-méthoprène
Les concentrations plasmatiques du S-méthoprène ont généralement été en-dessous de la limite de quantification (10 ng / mL) après application topique.
Le fipronil et son métabolite principal sont bien diffusés sur le pelage après administration topique.
Propriétés environnementales
Le produit ne doit pas entrer dans les cours d'eau car cela peut être dangereux pour les poissons et autres organismes aquatiques.
6. Informations pharmaceutiques
6.1. Liste des excipients
Butylhydroxyanisole (E320)
Butylhydroxytoluène (E321)
Ethanol anhydre
Ether monoéthylique de diéthylèneglycol
6.2. Incompatibilités majeures
Aucune connue.
6.3. Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
6.4. Précautions particulières de conservation
Pas de précautions particulières de conservation.
6.5. Nature et composition du conditionnement primaire
Pipette polyéthylène téréphtalate/polypropylène - polyéthylène téréphtalate/aluminium/polyester
6.6. Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
Le produit ne doit pas entrer dans les cours d'eau car cela peut être dangereux pour les poissons et autres organismes aquatiques.
7. Titulaire de l'autorisation de mise sur le marché
CEVA SANTE ANIMALE
10 AVENUE DE LA BALLASTIERE
33500 LIBOURNE
FRANCE
8. Numéro(s) d'autorisation de mise sur le marché
FR/V/3177846 0/2014
Boîte de 1 plaquette thermoformée de 1 pipette
Boîte de 3 plaquettes thermoformées de 1 pipette
Boîte de 6 plaquettes thermoformées de 1 pipette
Boîte de 12 plaquettes thermoformées de 1 pipette
Boîte de 24 plaquettes thermoformées de 1 pipette
Boîte de 60 plaquettes thermoformées de 1 pipette
Boîte de 120 plaquettes thermoformées de 1 pipette
Toutes les présentations peuvent ne pas être commercialisées.
9. Date de première autorisation/renouvellement de l'autorisation
24/02/2014 - 29/01/2019
10. Date de mise à jour du texte
20/03/2020