MOXICLEAR 400 MG + 100 MG SOLUTION POUR SPOT-ON POUR TRES GRANDS CHIENS
2. Composition qualitative et quantitative
Une pipette de 4 mL contient : |
|
|
|
Substance(s) active(s) : |
|
Imidaclopride ..................................................................... | 400 mg |
Moxidectine ....................................................................... | 100 mg |
|
|
Excipient(s) : |
|
Butylhydroxytoluène (E321) .............................................. | 4 mg |
Alcool benzylique ........................................................QSP. | 4 mL |
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
3. Forme pharmaceutique
Solution pour spot-on.
Solution incolore à jaune avec une légère opalescence.
4. Informations cliniques
4.1. Espèces cibles
Chiens.
4.2. Indications d'utilisation, en spécifiant les espèces cibles
Pour les chiens atteints ou exposés au risque d’infestations parasitaires mixtes :
- Prévention et traitement des infestations par les puces (Ctenocephalides felis),
- Traitement des infestations par les poux broyeurs (Trichodectes canis),
- Traitement de la gale des oreilles (Otodectes cynotis), de la gale sarcoptique (Sarcoptes scabiei var. canis),
- Prévention de la dirofilariose cardiaque (larves L3 et L4 de Dirofilaria immitis),
- Traitement des microfilaires circulatoires (Dirofilaria immitis),
- Traitement de la dirofilariose sous-cutanée (stade adulte de Dirofilaria repens),
- Prévention de la dirofilariose sous-cutanée (larves L3 de Dirofilaria repens),
- Réduction des micofilaires circulatoires (Dirofilaria repens),
- Prévention de l’angiostrongylose (larve L4 et adultes immatures d’Angiostrongylus vasorum),
- Traitement de l’angiostrongylose (Angiostrongylus vasorum) et de la crénosomose (Crenosoma vulpis),
- Prévention de la spirocercose (Spirocerca lupi),
- Traitement des infestations par les nématodes gastro-intestinaux (larves L4, adultes immatures et formes adultes de Toxocara canis, d’Ancylostoma caninum et d’Uncinaria stenocephala, et des formes adultes de Toxascaris leonina et de Trichuris vulpis).
Le médicament peut être intégré dans un programme thérapeutique de la Dermatite Allergique aux Piqûres de Puces (DAPP).
4.3. Contre-indications
Ne pas traiter les chiots de moins de 7 semaines.
Ne pas utiliser en cas d’hypersensibilité à l’une des substances actives ou à l’un des excipients.
Ne pas utiliser chez les chiens atteints de dirofilariose cardiaque classe 4 car l’innocuité de ce produit n’a pas été évaluée chez ce groupe d’animaux.
Pour les chats, la présentation correspondante du produit MOXICLEAR POUR CHATS (0,4 ou 0,8 mL), qui contient 100 mg/mL d’imidaclopride et 10 mg/mL de moxidectine doit être utilisée.
Pour les furets, ne pas utiliser MOXICLEAR POUR CHIENS. Utiliser uniquement MOXICLEAR POUR PETITS CHATS ET FURETS (0,4 mL).
Ne pas utiliser sur les canaris.
4.4. Mises en garde particulières à chaque espèce cible
Voir rubrique « Précautions particulières d’emploi ».
Un contact bref de l’animal avec l’eau une à deux fois entre les traitements mensuels ne réduira pas significativement l’efficacité du traitement. Cependant, des shampooings fréquents ou une immersion dans l’eau après traitement peuvent réduire l’efficacité du produit.
La résistance des parasites à une classe particulière d'anthelminthiques pourrait se développer suite à un usage fréquent et répété avec un anthelminthique appartenant à cette classe. Par conséquent, l’utilisation de ce produit devra être basée sur l’évaluation de chaque cas individuel et sur la situation épidémiologique locale concernant la sensibilité actuelle de l’espèce cible afin de limiter la possibilité d’une future sélection de résistance.
L’utilisation du produit doit être basée sur le diagnostic confirmé de l’infestation mixte (ou le risque d’infestation, dans le cas de la prévention) en même temps (voir rubriques « Indications d'utilisation, en spécifiant les espèces cibles » et « Posologie et voie d’administration »).
L’efficacité contre D. repens stade adulte n’a pas été démontrée.
4.5. Précautions particulières d'emploi
i) Précautions particulières d'emploi chez l'animal
Le traitement des animaux pesant moins de 1 kg devra être basé sur l’évaluation d’un rapport bénéfice/risque.
Compte tenu de l’expérience limitée quant à l’utilisation du produit chez les animaux malades ou affaiblis, le produit ne devra être administré chez ces animaux qu’après évaluation du rapport bénéfice/risque.
Éviter le contact du contenu de la pipette ou de la dose appliquée avec la bouche ou les yeux de l’animal traité ou des congénères. Veiller à ce que les animaux récemment traités ne puissent se lécher entre eux. Lorsque le médicament est appliqué en 3 ou 4 points, (voir rubrique « Posologie et voie d’administration »), veiller à ce que l’animal ne puisse pas lécher les sites d’application.
Ce produit contient de la moxidectine (lactone macrocyclique), aussi des précautions devront être prises avec les Colleys, les Bobtails et les races apparentées ou croisées afin d’administrer correctement le produit tel que décrit à la rubrique « Posologie et voie d’administration »; en particulier, l’ingestion orale par l’animal traité et/ou les autres animaux en contact direct devra être évitée.
L’innocuité du produit a seulement été évaluée chez des chiens atteints de dirofilariose cardiaque classe 1 ou 2 lors d’études de laboratoire ou chez quelques chiens en classe 3 lors d’une étude terrain. Par conséquent, l’utilisation de ce produit chez des chiens ayant des symptômes manifestes ou sévères de la maladie doit être basée sur l’évaluation soigneuse du rapport bénéfice/risque du vétérinaire traitant.
Bien que des études expérimentales en surdosage aient montré que le produit peut être administré en toute sécurité à des animaux infestés par des filaires adultes, il n’a pas d’effet thérapeutique contre les formes adultes de Dirofilaria immitis. Il est donc recommandé pour les animaux âgés de 6 mois ou plus, vivant dans des zones endémiques de Dirofilaria, de vérifier l’infestation par les filaires adultes avant de commencer le traitement. A la discrétion du vétérinaire, les chiens infestés doivent être traités avec un produit adulticide pour éliminer les filaires adultes. L’innocuité du médicament vétérinaire n’a pas été évaluée quand il est administré le même jour qu’un produit adulticide.
L’imidaclopride est toxique pour les oiseaux, notamment les canaris.
ii) Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Éviter tout contact avec la peau, les yeux ou la bouche.
Ne pas manger, boire ou fumer pendant l’application.
Bien se laver les mains après l’utilisation.
Après application, attendre que le site d’application soit sec pour caresser ou toiletter l’animal.
En cas de contact accidentel avec la peau, laver immédiatement avec de l’eau et du savon.
Les personnes présentant une hypersensibilité connue à l’alcool benzylique, l’imidaclopride ou la moxidectine doivent manipuler le produit avec précaution. Dans de très rares cas, le produit pourra être à l’origine de sensibilisation cutanée ou de réactions cutanées transitoires (par exemple engourdissement, irritation ou sensation de brûlure/picotement).
Dans de très rares cas, le produit peut provoquer une irritation respiratoire chez des individus sensibles.
En cas de contact oculaire accidentel, rincer abondamment les yeux à l’eau.
Si une irritation oculaire ou cutanée persiste, ou en cas d’ingestion accidentelle du médicament vétérinaire, prenez immédiatement conseil auprès de votre médecin et montrez-lui la notice ou l’étiquette.
Ne pas ingérer. En cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Afin d’éviter que les enfants entrent en contact avec les pipettes, gardez la pipette dans l’emballage d’origine jusqu’à ce que vous soyez prêt à l’utiliser et jetez immédiatement les pipettes usagées.
Ne pas manipuler les animaux traités et ne pas autoriser les enfants à jouer avec les animaux traités jusqu'à ce que le site d'application soit sec. Il est par conséquent recommandé que les animaux ne soient pas traités dans la journée, mais plutôt en début de soirée et que les animaux récemment traités ne soient pas autorisés à dormir avec les propriétaires, surtout les enfants.
iii) Autres précautions
Le médicament vétérinaire ne doit pas pouvoir entrer en contact avec les cours d’eau car il peut avoir des effets néfastes sur les organismes aquatiques : la moxidectine est hautement toxique pour les organismes aquatiques. Ne pas laisser les chiens se baigner dans des cours d’eau pendant au moins les quatre jours suivant l’administration du traitement.
Le solvant du médicament vétérinaire pourrait marquer ou endommager certains matériaux tels que cuir, tissus plastiques ou surfaces vernies. S’assurer que le site d’application est sec avant tout contact avec l’un de ces matériaux.
4.6. Effets indésirables (fréquence et gravité)
L’utilisation de ce médicament chez les chiens peut entraîner un prurit transitoire. Dans de rares cas un poil gras, un érythème ou des vomissements peuvent apparaître. Ces signes disparaissent sans aucun traitement. Le médicament peut dans de rares cas provoquer des réactions locales d’hypersensibilité. Si l’animal lèche le site d’application, des signes neurologiques (la plupart transitoires) peuvent être observés dans de très rares cas (voir rubrique « Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire »).
La solution a une saveur amère. Une salivation peut apparaître occasionnellement si l’animal lèche le site d’application, immédiatement après le traitement. Il ne s’agit pas d’un signe d’intoxication et cet effet disparaît en quelques minutes sans aucun traitement. Une application correcte diminuera les possibilités de léchage du site d’application.
Dans de très rares cas, le produit peut provoquer sur le site d’application une sensation qui peut être à l’origine de comportements transitoires tels que léthargie, agitation et inappétence.
Une étude terrain a montré que chez les chiens atteints de dirofilariose cardiaque avec microfilarémie, il y a un risque de signes respiratoires sévères (toux, tachypnée et dyspnée) pouvant nécessiter un traitement vétérinaire rapide. Dans cette étude, ces réactions étaient fréquentes (observées chez 2 des 106 chiens traités). Des signes gastro-intestinaux (vomissements, diarrhées, inappétence) et léthargie sont également des effets indésirables fréquents après traitement de ces chiens.
La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
4.7. Utilisation en cas de gestation, de lactation ou de ponte
L’innocuité du médicament n’a pas été établie en cas de gestation et de lactation.
Les études en laboratoire menées avec l’imidaclopride ou la moxidectine sur le rat et le lapin n’ont pas mis en évidence d’effets tératogènes, foetotoxiques ou maternotoxiques.
L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
4.8. Interactions médicamenteuses et autres formes d'interactions
Pendant le traitement avec le médicament vétérinaire, aucun autre antiparasitaire de la famille des lactones macrocycliques ne doit pas être administré.
Aucune interaction entre ce médicament vétérinaire et les médicaments vétérinaires d’usage courant, les interventions chirurgicales ou médicales n’a été observée.
L’innocuité du médicament vétérinaire administré le même jour qu’un produit adulticide pour éliminer les filaires cardiaques adultes n’a pas été évaluée.
4.9. Posologie et voie d'administration
Schéma posologique
La dose minimale recommandée est de 10 mg d’imidaclopride et 2,5 mg de moxidectine /kg de poids corporel, équivalent à 0,1 mL de ce produit /kg de poids corporel.
Le programme de traitement devra être basé sur le diagnostic individuel du vétérinaire et sur la situation épidémiologique locale.
Poids du Chien | Taille de la pipette à utiliser | Volume | Imidaclopride [mg/kg] | Moxidectine [mg/kg] |
≤ 4 kg | MOXICLEAR POUR PETITS CHIENS | 0,4 mL | minimum10 | minimum 2,5 |
> 4 – ≤ 10 kg | MOXICLEAR POUR CHIENS MOYENS | 1 mL | 10–25 | 2,5–6,25 |
> 10 – ≤ 25 kg | MOXICLEAR POUR GRANDS CHIENS | 2,5 mL | 10–25 | 2,5–6,25 |
> 25 – ≤ 40 kg | MOXICLEAR POUR TRÈS GRANDS CHIENS | 4 mL | 10–16 | 2,5–4 |
> 40 kg | Association appropriée de pipettes | |||
Prévention et traitement des infestations par les puces (Ctenocephalides felis)
Un seul traitement prévient les réinfestations futures par les puces pendant 4 semaines. Les pupes déjà présentes dans l’environnement pourront continuer à se développer pendant 6 semaines ou plus après le début du traitement selon les conditions climatiques. Aussi, il pourrait être nécessaire de combiner le traitement avec le du produit avec des traitements de l’environnement visant à interrompre le cycle de la puce dans l’environnement de l’animal. Cela peut permettre de réduire plus rapidement la population de puces dans le foyer.
Le produit devra être administré une fois par mois lorsqu’il est intégré dans un programme thérapeutique de la Dermatite Allergique aux Piqûres de Puces (DAPP).
Traitement des infestations par les poux broyeurs (Trichodectes canis)
Administrer une dose unique. Une visite de contrôle chez le vétérinaire 30 jours après l’application est conseillée car une seconde application peut être nécessaire chez certains chiens.
Traitement de la gale des oreilles (Otodectes cynotis)
Administrer une dose unique de médicament. Lors de chaque traitement, nettoyer doucement pour retirer les saletés du conduit auditif externe. Une visite de contrôle chez le vétérinaire 30 jours après l’application est conseillée car une seconde application peut être nécessaire chez certains chiens. Ne pas appliquer directement dans le conduit auditif.
Traitement de la gale sarcoptique (Sarcoptes scabiei var. canis)
Administrer une dose unique du médicament, deux fois à 4 semaines d’intervalle.
Prévention de la dirofilariose cardiaque (D. immitis) et de la dirofilariose sous-cutanée (ver cutané)(D. repens)
Les chiens vivant dans des régions endémiques, ou ceux qui ont voyagé dans des régions endémiques de Dirofilaria, peuvent être infestés par les formes adultes de parasites. En conséquence, avant d’administrer le médicament, tenir compte des conseils de la rubrique « Précautions particulières d’emploi ».
Pour une prévention de la dirofilariose cardiaque et de la dirofilariose sous-cutanée, le médicament doit être appliqué tous les mois pendant la période d’exposition aux moustiques (hôtes intermédiaires qui portent et transmettent les larves de D. immitis et D. repens). Le produit pourra être administré tout au long de l’année, ou au moins un mois avant la première exposition attendue aux moustiques. Le traitement devra être ensuite administré mensuellement et ce jusqu’à 1 mois après la fin de la période d’exposition aux moustiques.
Pour garantir la périodicité des traitements, il est recommandé d’appliquer le produit le même jour de chaque mois, ou à une date fixe du mois.
Lorsque le médicament est administré en remplacement d’un autre traitement préventif de la Dirofilariose dans un programme de prévention de la dirofilariose, le premier traitement avec le médicament vétérinaire devra être administré dans le mois suivant l’application de la dernière dose du traitement précédent.
Dans les régions non-endémiques, les chiens n’ont pas de risque de contracter la Dirofilariose. Aussi, ils pourront être traités sans précaution particulière.
Traitement des microfilaires (D. immitis)
Administrer le produit une fois par mois pendant deux mois consécutifs.
Traitement de la dirofilariose sous-cutanée (ver cutané) (stade adulte de Dirofilaria repens)
Administrer le produit une fois par mois pendant six mois consécutifs.
Réduction des microfilaires (D. repens)
Le produit doit être administré tous les mois pendant 4 mois consécutifs. L’efficacité contre les vers adultes n’a pas été montrée. Les vers adultes pourraient continuer à produire des microfilaires.
Traitement et prévention de l’angiostrongylose (Angiostrongylus vasorum)
Administrer une dose unique du médicament. Une visite de contrôle chez le vétérinaire 30 jours après l’application est conseillée car une seconde application peut être nécessaire chez certains animaux.
Dans les zones endémiques, une application régulière toutes les 4 semaines préviendra l’angiostrongylose et les infestations patentes d’Angiostrongylus vasorum.
Traitement de la crénosomose (Crenosoma vulpis)
Administrer une dose unique.
Prévention de la spirocercose Spirocerca lupi
Le produit doit être administré mensuellement.
Traitement des infestations par les ascarides, ankylostomes et trichures (Toxocara canis, Ancylostoma caninum, Uncinaria stenocephala, Toxascaris leonina et Trichuris vulpis)
Dans les zones endémiques de Dirofilaria, l’application d’un traitement mensuel réduira significativement le risque de réinfestation causée respectivement par les ascarides, les ankylostomes et les trichures. Dans les régions non-endémiques de Dirofilaria, le produit peut être utilisé dans le cadre d’un programme saisonnier de prévention contre les infestations par les puces ou les nématodes gastro-intestinaux.
Des études ont montré que les traitements mensuels des chiens préviennent les infestations causées par Uncinaria stenocephala.
Mode d’Administration
Uniquement pour un usage externe.
Ne pas sortir la pipette du sachet avant d’être prêt à l’utiliser.
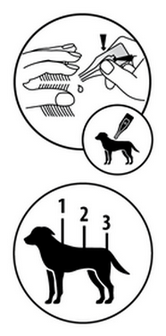
Retirer la pipette du sachet soit en utilisant des ciseaux, soit en pliant le long de la ligne diagonale pour exposer l’encoche prévue puis en déchirant le sachet au niveau de l’encoche.
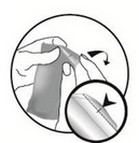
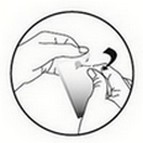
Tenir la pipette en position verticale. Tapoter la partie étroite de la pipette pour s’assurer que soncontenu se trouve à dans de la partie principale de la pipette. Tordre l’extrémité de la pipette.
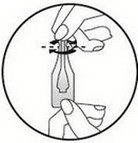
Pour les chiens de25 kg ou moins:
Tenir le chien en position debout, écarter les poils du dos de l’animal à la base du cou, devant les omoplates, jusqu’à ce que la peau soit visible. Appliquer si possible sur une peau saine. Placer l’extrémité de la pipette sur la peau et appuyer plusieurs fois pour en vider entièrement le contenu, directement sur la peau.
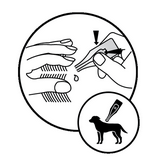
Pour les chiens de plus de 25 kg:
Pour une application aisée, le chien sera maintenu en position debout.
Tout contenu de la pipette sera réparti en 3 ou 4 points sur la ligne du dos, depuis les épaules jusqu’à la base de la queue. A chaque point, le poil sera écarté jusqu’à ce que la peau soit visible. Appliquer si possible sur une peau saine. Placer l’extrémité de la pipette sur la peau et presser doucement la pipette de manière à appliquer une partie de son contenu directement sur la peau du chien. Ne pas appliquer une trop grande quantité de produit par point d’application afin d’éviter que la solution ne coule sur les flancs de l’animal.
4.10. Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
L’application de doses jusqu’à 10 fois la dose recommandée a été bien tolérée chez les chiens adultes sans aucun effet ou signe clinique indésirable. L’application de 5 fois la dose minimale recommandée à des intervalles d’une semaine pendant 17 semaines a été étudiée chez des chiens âgés de plus de 6 mois et a été bien toléré sans aucun effet ou signe clinique indésirable.
Le produit a été administré à des chiots toutes les 2 semaines, pendant 6 traitements, jusqu’à 5 fois la dose recommandée et aucun trouble sérieux n’a été relevé. Une mydriase transitoire, de la salivation, des vomissements et une accélération respiratoire passagère ont pu être observés.
Après une ingestion accidentelle ou un surdosage, des signes neurologiques (la plupart transitoires) tels qu’ataxie, des tremblements généralisés, des signes oculaires (pupilles dilatées, réflexe pupillaire diminué, nystagmus), une respiration anormale, une salivation et des vomissements peuvent survenir dans de très rares cas.
Les Colleys sensibles à l’ivermectine ont toléré jusqu’à 5 fois la dose recommandée répétée à des intervalles d’un mois sans aucun effet indésirable, mais la sécurité de l'application à des intervalles d'une semaine n'a pas été étudiée chez les Colleys sensibles à l’ivermectine. Après administration orale de 40% d’une dose unitaire, des signes neurologiques sévères ont pu être observés. L’administration orale de 10% d’une dose unitaire n’a provoqué aucun effet indésirable.
Les chiens infestés par des formes adultes de Dirofilaria immitis ont toléré sans effet indésirable jusqu’à 5 fois la dose recommandée administrée 3 fois toutes les deux semaines.
En cas d’ingestion accidentelle, un traitement symptomatique devra être administré. Il n’y a pas d’antidote spécifique connu. L’utilisation de charbon actif pourra être bénéfique.
4.11. Temps d'attente
Sans objet.
5. Propriétés pharmacologiques
Groupe pharmacothérapeutique: produits antiparasitaires, insecticides et répulsifs, lactones macrocycliques, milbémycines.
Code ATC-vet : QP54AB52.
5.1. Propriétés pharmacodynamiques
L’imidaclopride, 1-(6-Chloro-3-pyridylmethyl)-N-nitro-imidazolidin-2-ylideneamine est un antiparasitaire externe appartenant à la famille des chloronicotiniles. Du point de vue chimique, il s’agit plus précisément d’un chloronicotinyl nitroguanidine. L’imidaclopride est actif contre les stades larvaires et adultes des puces. Les larves de puces présentes dans l’environnement de l’animal sont tuées par contact avec l’animal traité avec le médicament vétérinaire. L’imidaclopride possède une forte affinité pour les récepteurs nicotiniques de l’acétylcholine de la région post-synaptique du système nerveux central (SNC) de la puce. L’inhibition de la transmission cholinergique qui s’ensuit conduit à la paralysie et la mort des insectes. De par sa faible affinité pour les récepteurs nicotiniques des mammifères et son faible passage supposé de la barrière hémato-méningée de ceux-ci, l’imidaclopride n’a pas d’effet sur le système nerveux central des mammifères. L’imidaclopride a une activité pharmacologique minimale chez les mammifères.
La moxidectine, 23-(O-methyloxime)-F28249 Alpha est une lactone macrocyclique de seconde génération de la famille des milbémycines. C’est un antiparasitaire actif contre une large gamme de parasites externes et internes. La moxidectine est active contre les stades larvaires (L3, L4) de Dirofilaria immitis. Elle est également active sur les nématodes gastro-intestinaux. La moxidectine agit par interférence avec les récepteurs GABA et les canaux à ions chlorures dépendants du glutamate. L’effet résultant est l’ouverture des canaux chlore de la jonction postsynaptique pour permettre l’entrée des ions chlore et l’induction d’un état de repos irréversible. Ceci provoque une paralysie flasque des parasites exposés suivie par leur mort et/ou leur expulsion.
5.2. Caractéristiques pharmacocinétiques
Après application topique du médicament vétérinaire, l’imidaclopride se répartit rapidement sur la peau de l’animal dans le jour suivant l’application. Il peut être détecté sur la surface du corps pendant l’intervalle entre traitements.
La moxidectine est absorbée par voie cutanée, et atteint des concentrations plasmatiques maximales en 4 à 9 jours environ après traitement chez le chien. Après absorption à partir de la peau, la moxidectine est distribuée par voie systémique, et est lentement éliminée du plasma comme en attestent les concentrations plasmatiques détectables pendant l’intervalle entre deux traitements mensuels.
Propriétés environnementales
Voir rubrique « Précautions particulières d’emploi » et « Précautions particulières à prendre lors de l’élimination de médicaments vétérinaires non utilisés ou des déchets dérivés de l’utilisation de ces médicaments ».
6. Informations pharmaceutiques
6.1. Liste des excipients
Butylhydroxytoluène (E321)
Alcool benzylique
Carbonate de propylène
6.2. Incompatibilités majeures
Aucune connue.
6.3. Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 2 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
Conserver dans l’emballage extérieur de façon à protéger de la lumière et de l’humidité.
6.5. Nature et composition du conditionnement primaire
Pipette moulée à partir d’un film en polypropylène / COC – laminé laqué sans solvant– copolymère de polyéthylène / EVOH / polyéthylène
6.6. Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Le médicament vétérinaire ne doit pas être déversé dans les cours d’eau car cela pourrait mettre en danger les poissons et autres organismes aquatiques.
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
7. Titulaire de l'autorisation de mise sur le marché
NORBROOK LABORATORIES (IRELAND)
ROSSMORE INDUSTRIAL ESTATE
- MONAGHAN
IRLANDE
8. Numéro(s) d'autorisation de mise sur le marché
FR/V/7754419 9/2018
Boîte de 1 sachet de 1 pipette de 4,0 mL
Boîte de 2 sachets de 1 pipette de 4,0 mL
Boîte de 3 sachets de 1 pipette de 4,0 mL
Boîte de 4 sachets de 1 pipette de 4,0 mL
Boîte de 6 sachets de 1 pipette de 4,0 mL
Boîte de 9 sachets de 1 pipette de 4,0 mL
Boîte de 12 sachets de 1 pipette de 4,0 mL
Boîte de 21 sachets de 1 pipette de 4,0 mL
Boîte de 42 sachets de 1 pipette de 4,0 mL
Toutes les présentations peuvent ne pas être commercialisées.
9. Date de première autorisation/renouvellement de l'autorisation
24/05/2018 - 28/01/2022
10. Date de mise à jour du texte
09/02/2023