SELASPOT 120 MG SOLUTION POUR SPOT-ON POUR CHIENS 10,1 - 20 KG
2. Composition qualitative et quantitative
Une pipette de 1 mL contient : |
|
|
|
Substance(s) active(s) : |
|
Sélamectine …………………………………………... | 120 mg |
|
|
Excipient(s) : |
|
Butylhydroxytoluène (E321) ………………………… | 0,8 mg |
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
3. Forme pharmaceutique
Solution pour spot-on.
Solution limpide et incolore à légèrement jaune.
4. Informations cliniques
4.1. Espèces cibles
Chiens (10,1 – 20,0 kg).
4.2. Indications d'utilisation, en spécifiant les espèces cibles
Traitement et prévention des infestations par les puces dues à Ctenocephalides spp. pendant un mois après l’administration d’une dose unique. Ceci grâce à l’activité adulticide, larvicide et ovicide du médicament. Le produit a une activité ovicide pendant les 3 semaines suivant son administration. En réduisant la quantité de puces, le traitement mensuel des femelles gestantes et allaitantes aide aussi à prévenir l’infestation de la portée par les puces jusqu’à l’âge de sept semaines. Le produit peut être intégré dans un programme thérapeutique contre la dermatite allergique aux piqûres de puces (DAPP et, grâce à son activité ovicide et larvicide, peut contribuer à enrayer les infestations existantes dans l’environnement de l’animal.
Prévention de la dirofilariose due à Dirofilaria immitis par administration mensuelle.
Traitement de la gale des oreilles (Otodectes cynotis).
Traitement des infestations par les poux broyeurs (Trichodectes canis).
Traitement de la gale sarcoptique (due à Sarcoptes scabiei).
Traitement des ascaridioses intestinales dues aux formes adultes des ascaris (Toxocara canis).
4.3. Contre-indications
Ne pas utiliser chez les animaux âgés de moins de 6 semaines.
Ne pas utiliser chez des animaux atteints de maladies concomitantes, ou affaiblis et d’un poids insuffisant (pour leur taille et leur âge).
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
4.4. Mises en garde particulières à chaque espèce cible
Les animaux peuvent être lavés 2 heures après le traitement sans perte d’efficacité.
Ne pas appliquer si le poil de l’animal est mouillé. Cependant, un shampooing ou une baignade de l’animal 2 heures ou plus après le traitement ne réduira pas l’efficacité du produit.
Pour le traitement de la gale des oreilles, ne pas administrer directement dans le conduit auditif.
Il est important d’appliquer le traitement comme indiqué afin de limiter la quantité que l’animal pourrait ingérer par léchage.
Le produit peut être administré en toute sécurité à des animaux infestés par des filaires cardiaques adultes. Cependant, conformément aux bonnes pratiques vétérinaires, tous les animaux âgés d’au moins 6 mois et vivant dans des pays où un vecteur existe doivent être examinés afin de déceler une éventuelle infestation par des filaires adultes avant d’initier le traitement. Il est également recommandé de vérifier régulièrement que les animaux ne soient pas porteurs de filaires cardiaques adultes, dans le cadre d'une stratégie complète de prévention contre la dirofilariose, même lorsque le produit est appliqué mensuellement. Ce produit n’est pas efficace vis-à-vis des formes adultes de D. immitis.
La résistance des parasites à une classe particulière d’anthelminthiques peut se développer après une utilisation fréquente et répétée d’un anthelminthique de cette même classe. Par conséquent, l’utilisation de ce médicament vétérinaire doit être basée sur l’évaluation de chaque cas individuel et sur les informations épidémiologiques locales concernant la sensibilité actuelle de l’espèce cible afin de limiter le risque d’émergence de résistance aux antihelminthiques.
4.5. Précautions particulières d'emploi
i) Précautions particulières d'emploi chez l'animal
Ce médicament vétérinaire doit être appliqué seulement sur la peau. Il ne doit pas être administré par voie orale ou parentérale.
Éloigner les animaux traités de toute flamme ou autre source de combustion au moins pendant les 30 minutes qui suivent l’application du produit ou jusqu’au séchage des poils au niveau de la zone traitée.
ii) Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le produit est nocif après ingestion. Conserver le produit dans son emballage d’origine jusqu’à son utilisation, afin d’éviter que les enfants n’aient un accès direct au produit. Les pipettes usagées doivent être éliminées immédiatement et ne pas être laissées à la vue ou à la portée des enfants. En cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Le produit est irritant pour la peau et les yeux. Éviter tout contact avec les yeux, y compris le contact entre les mains et les yeux. Se laver les mains après utilisation et en cas de contact accidentel avec la peau, laver immédiatement la zone atteinte à l'eau et au savon. En cas de contact accidentel avec les yeux, les rincer immédiatement à l’eau, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Les animaux traités ne doivent pas être manipulés pendant au moins 12 heures après l’application du produit. Il est donc recommandé de traiter l’animal le soir. Le jour du traitement, les animaux traités ne doivent pas être autorisés à dormir avec leurs propriétaires, particulièrement les enfants.
Ne pas fumer, manger ou boire pendant la manipulation du produit.
Les personnes ayant une peau sensible ou présentant une allergie connue à ce type de médicament vétérinaire doivent manipuler le produit avec précaution.
Le produit est hautement inflammable. Conserver à l’abri de la chaleur, des étincelles, d’une flamme ou de toute autre source de combustion.
iii) Autres précautions
La sélamectine est toxique pour les organismes aquatiques. Les chiens traités ne doivent pas être autorisés à se baigner dans les cours d’eau pendant 48 heures après le traitement, afin d’éviter les effets indésirables sur les organismes aquatiques.
4.6. Effets indésirables (fréquence et gravité)
Dans de rares cas, l’administration du médicament vétérinaire peut entraîner temporairement et localement au site d’application la formation d'une touffe de poils agglutinés et/ou l’apparition d’une petite quantité de poudre blanche. Ce phénomène est normal et disparaîtra généralement dans les 24 heures suivant l’administration du médicament et n’affecte ni l’efficacité, ni l’innocuité du médicament.
Très rarement, comme avec d’autres lactones macrocycliques, des signes neurologiques réversibles, y compris des convulsions, ont été observés après utilisation du médicament vétérinaire chez les chiens.
La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
4.7. Utilisation en cas de gestation, de lactation ou de ponte
Le produit peut être utilisé chez les chiens pendant la gestation, la lactation et la reproduction.
4.8. Interactions médicamenteuses et autres formes d'interactions
Aucune connue.
4.9. Posologie et voie d'administration
Méthode et voie d’administration
Application externe (spot-on).
Appliquer le médicament sur la peau, à la base du cou, en avant des omoplates.
Le produit doit être administré en une application unique délivrant au minimum 6 mg de sélamectine / kg. Quand plusieurs infestations ou infections pouvant être traitées par le médicament vétérinaire affectent un même animal, l’administration unique à la dose de 6 mg de sélamectine / kg est recommandée. L'intervalle de temps entre deux administrations du médicament, pour chaque indication concernée, est indiqué ci-dessous.
Administrer le produit conformément au tableau suivant :
Chiens (kg) | Couleur du capuchon de la pipette | Dose de sélamectine administrée en mg | Concentration (mg/mL) | Volume administré (taille nominale des pipettes, mL) |
10,1 – 20,0 | Rouge | 120 | 120 | 1,0 |
Traitement et prévention des infestations par les puces
Après administration du médicament vétérinaire, les puces adultes présentes sur l’animal sont tuées, les œufs pondus ne sont plus viables et les larves (présentes seulement dans l’environnement) sont également tuées. La reproduction des puces est stoppée, leur cycle de vie interrompu et cela peut contribuer à contrôler les infestations existantes dans l’environnement de l’animal.
Pour la prévention des infestations par les puces, le médicament vétérinaire doit être administré tous les mois pendant la saison des puces, en commençant un mois avant que les puces ne deviennent actives. En réduisant la quantité de puces, le traitement mensuel des femelles gestantes et allaitantes aide à prévenir l’infestation de la portée par les puces jusqu’à l’âge de sept semaines.
Intégré dans un programme thérapeutique contre la Dermatite Allergique aux Piqûres de Puces (DAPP), le médicament vétérinaire doit être administré selon un rythme mensuel.
Prévention de la dirofilariose
La nécessité d’un traitement doit être déterminée par le vétérinaire prescripteur et doit être basée sur la situation épidémiologique locale (voir rubrique « Mises en garde particulières à chaque espèce cible »). Pour la prévention de la dirofilariose, le médicament vétérinaire doit être administré dans le mois suivant la première exposition de l’animal aux moustiques puis tous les mois jusqu’à un mois après la dernière exposition aux moustiques. En cas d'oubli d'un des traitements mensuels et si l’intervalle d’un mois entre deux applications est dépassé, l’administration immédiate du médicament vétérinaire et le retour à un rythme mensuel d’administration minimiseront les risques de développement des formes adultes de Dirofilaria immitis. La nécessité d’un traitement prolongé doit être déterminée par le vétérinaire prescripteur. Dans le cadre d’un programme de prévention de la dirofilariose, lorsqu’on remplace un autre médicament anti-dirofilariose par ce médicament vétérinaire, la première dose de ce médicament doit être administrée dans le mois suivant la dernière dose du traitement précédent.
Traitement des ascaridioses
Le traitement consiste en une administration unique du médicament vétérinaire.
Traitement des infestations par les poux broyeurs
Le traitement consiste en une administration unique du médicament vétérinaire.
Traitement de la gale des oreilles
Le traitement consiste en une administration unique du médicament vétérinaire. Il est recommandé de retirer doucement les débris du conduit auditif externe avant chaque administration. Une visite de contrôle chez le vétérinaire 30 jours après l’application est conseillée car une seconde application peut être nécessaire chez certains animaux.
Traitement de la gale sarcoptique
Pour l’élimination complète des parasites, le médicament vétérinaire doit être administré deux fois, à 1 mois d’intervalle.
Mode d’utilisation :
Retirer la pipette de sa plaquette de protection.
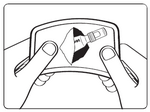
En tenant la pipette bien droite, appuyer fermement sur son capuchon pour perforer l’opercule de protection de l’applicateur, puis enlever le capuchon.
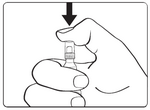
Écarter les poils de l’animal afin de libérer une petite zone de peau nue à la base du cou, en avant des omoplates.
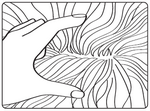
Placer alors le bout de la pipette directement sur la zone de peau ainsi mise à nu, sans effectuer de massage. Presser alors fermement la pipette pour la vider totalement de son contenu en un seul point d’application. Éviter tout contact entre le produit et vos doigts.

4.10. Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Aucun effet indésirable n’a été observé après l’administration de 10 fois la dose recommandée de sélamectine. La sélamectine a été administrée à 3 fois la dose recommandée à des chiens parasités par des filaires cardiaques adultes, sans qu’apparaissent d’effets indésirables. La sélamectine a aussi été administrée à 3 fois la dose recommandée à des chiens mâles et femelles reproducteurs, dont des femelles gestantes ou allaitant leurs portées, et à 5 fois la dose recommandée à des Colleys sensibles à l’ivermectine, sans qu’apparaissent d’effets indésirables.
4.11. Temps d'attente
Sans objet.
5. Propriétés pharmacologiques
Groupe pharmacothérapeutique : agent antiparasitaire, insecticide et répulsif, lactones macrocycliques.
Code ATC-vet : QP54AA05.
5.1. Propriétés pharmacodynamiques
La sélamectine est un composé semi-synthétique de la classe des avermectines. La sélamectine paralyse et/ou tue un large éventail de parasites invertébrés en modifiant la perméabilité des membranes cellulaires aux ions chlorures, ce qui perturbe la neurotransmission. Par conséquent, l’activité électrique des cellules nerveuses des nématodes et celle des cellules musculaires des arthropodes sont inhibées conduisant à leur paralysie et/ou leur mort.
La sélamectine a une activité adulticide, ovicide et larvicide contre les puces. Elle interrompt donc efficacement le cycle de vie de la puce en tuant les adultes (sur l’animal), en empêchant l’éclosion des œufs (sur l’animal et dans son environnement) et en tuant les larves (seulement dans l’environnement). Les débris issus des animaux traités par la sélamectine tuent les œufs et les larves de puces qui n’ont pas été préalablement exposés à la sélamectine et peuvent donc contribuer à contrôler les infestations existantes dans l’environnement de l’animal.
L’activité larvicide de la sélamectine sur les filaires cardiaques a aussi été démontrée.
5.2. Caractéristiques pharmacocinétiques
Après administration cutanée, la sélamectine est absorbée par la peau et atteint sa concentration plasmatique maximale en environ 3 jours chez le chien.
Après absorption cutanée, la sélamectine se distribue de façon systémique et s’élimine lentement du plasma comme le démontre l’existence chez le chien de concentrations plasmatiques détectables 30 jours après l’administration cutanée d’une dose unique de 6 mg/kg. La persistance prolongée de la sélamectine dans le plasma et sa lente élimination se traduisent par des demi-vies d’élimination terminales de 11 jours respectivement chez le chien. La persistance systémique de la sélamectine dans le plasma et sa faible transformation métabolique permettent d’avoir des concentrations efficaces de sélamectine durant l’intervalle de temps requis entre deux administrations (30 jours).
6. Informations pharmaceutiques
6.1. Liste des excipients
Butylhydroxytoluène (E321)
Éther monométhylique de dipropylèneglycol
Alcool isopropylique
6.2. Incompatibilités majeures
Aucune connue.
6.3. Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
6.4. Précautions particulières de conservation
Conserver dans l’emballage d’origine de façon à protéger de la lumière.
À conserver dans un endroit sec.
À conserver à une température ne dépassant pas 25 C.
6.5. Nature et composition du conditionnement primaire
Pipette unidose polypropylène avec un bouchon rouge dans une plaquette aluminium
6.6. Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Tous médicaments vétérinaires non utilisés ou déchets dérivés de ces médicaments doivent être éliminés conformément aux exigences locales.
Le produit ne doit pas être déversé dans les cours d’eau car cela pourrait mettre en danger les poissons et autres organismes aquatiques. Les récipients et reliquats de produit doivent donc être éliminés via la collecte des ordures ménagères afin de ne pas polluer les cours d’eau.
7. Titulaire de l'autorisation de mise sur le marché
BIMEDA ANIMAL HEALTH
UNIT 2/3/4 AIRTON CLOSE
TALLAGHT
DUBLIN 24 DUBLIN
IRLANDE
8. Numéro(s) d'autorisation de mise sur le marché
FR/V/7581036 2/2023
Boîte de 3 plaquettes de 1 pipette de 1 mL
Boîte de 6 plaquettes de 1 pipette de 1 mL
Toutes les présentations peuvent ne pas être commercialisées.
9. Date de première autorisation/renouvellement de l'autorisation
29/03/2023
10. Date de mise à jour du texte
29/03/2023