TRAMADOG TVM COMPRIME POUR CHIENS
2. Composition qualitative et quantitative
Chaque comprimé contient : |
|
|
|
Substance(s) active(s) : |
|
Tramadol………………………………………………….. | 43,90 mg |
(sous forme de chlorhydrate) |
|
(équivalant à 50 mg de chlorhydrate de tramadol) |
|
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
3. Forme pharmaceutique
Comprimé.
Comprimé blanc à crème, légèrement tacheté, rond et convexe, de 10 mm, portant une barre de sécabilité en forme de croix.
Les comprimés peuvent être divisés en 2 ou 4 parties égales.
4. Informations cliniques
4.1. Espèces cibles
Chiens.
4.2. Indications d'utilisation, en spécifiant les espèces cibles
Réduction des douleurs aiguës et chroniques peu intenses des tissus mous et du système musculo-squelettique.
4.3. Contre-indications
Ne pas administrer conjointement avec des antidépresseurs tricycliques, des inhibiteurs de la monoamine oxydase et des inhibiteurs de la recapture de la sérotonine.
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
Ne pas utiliser chez les animaux souffrant d’épilepsie.
4.4. Mises en garde particulières à chaque espèce cible
Les effets analgésiques du chlorhydrate de tramadol peuvent être variables. Cette variabilité serait due à des différences individuelles au niveau du métabolisme du médicament qui aboutit au métabolite actif principal, le O-déméthyltramadol. Chez certains chiens (ne répondant pas au traitement), le produit peut ainsi ne pas produire l'effet analgésique souhaité. En cas de douleur chronique, une analgésie multimodale doit être envisagée. Les chiens doivent être surveillés régulièrement par un vétérinaire afin d’assurer un soulagement adéquat de la douleur. En cas de réapparition de la douleur ou d’une analgésie insuffisante, il peut s’avérer nécessaire de revoir le protocole analgésique.
4.5. Précautions particulières d'emploi
i) Précautions particulières d'emploi chez l'animal
Les comprimés étant aromatisés, les conserver hors d’atteinte des animaux afin d’éviter toute ingestion accidentelle.
Le comprimé n’est adapté uniquement qu’aux chiens pesant plus de 3,12 kg.
Utiliser avec précaution chez les chiens présentant une insuffisance rénale ou hépatique. Chez les chiens présentant une insuffisance hépatique, le métabolisme du tramadol conduisant à la formation des métabolites actifs peut être réduit, ce qui peut diminuer l’efficacité du produit. L’un des métabolites actifs du tramadol étant excrété par voie rénale, il peut être nécessaire d’ajuster la posologie chez les chiens présentant une insuffisance rénale. La fonction rénale et la fonction hépatique doivent être surveillées lors de l’utilisation de ce produit. L’arrêt d’un traitement analgésique de longue durée doit se faire progressivement, quand cela est possible.
ii) Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le tramadol peut provoquer de la sédation, des nausées et des étourdissements après une ingestion accidentelle, en particulier chez l’enfant.
Afin d’éviter toute ingestion accidentelle, notamment chez l’enfant, remettre les fractions de comprimé inutilisées dans l’alvéole ouverte de la plaquette thermoformée, puis replacer cette dernière dans la boîte et conserver cette dernière hors de la vue et de la portée des enfants.
En cas d’ingestion accidentelle, en particulier chez l’enfant, consulter immédiatement un médecin et lui montrer la notice ou l’étiquette. En cas d’ingestion accidentelle chez l’adulte : ne pas conduire car des effets sédatifs sont possibles.
Les personnes présentant une hypersensibilité connue au tramadol ou à l’un des excipients doivent éviter le contact avec le médicament vétérinaire.
Se laver les mains après utilisation.
iii) Autres précautions
Aucune.
4.6. Effets indésirables (fréquence et gravité)
Il est fréquent qu’une légère sédation et de la somnolence surviennent, en particulier si des doses élevées sont administrées.
Des nausées et de vomissements ont été observés peu fréquemment chez les chiens après l’administration du tramadol.
Dans de rares cas, une réaction d’hypersensibilité peut se produire. En cas de réactions d’hypersensibilité, le traitement doit être interrompu.
Dans de très rares cas, le tramadol peut induire des convulsions chez les chiens à seuil épileptogène bas.
La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
4.7. Utilisation en cas de gestation, de lactation ou de ponte
Gestation :
Les études de laboratoire menées avec du tramadol chez la souris et/ ou le rat et le lapin, respectivement, n’ont pas mis en évidence d’effets tératogènes, fœtotoxiques ou maternotoxiques. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
Lactation :
Au cours des études de laboratoire menées avec du tramadol chez la souris et/ ou le rat et le lapin, respectivement, n’ont pas mis en évidence d’effet délétère sur le développement périnatal et postnatal de la progéniture. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
Fertilité :
Lors des études de laboratoire sur la souris et/ ou le rat et le lapin, respectivement, l’utilisation du tramadol aux doses thérapeutiques n’a pas eu d’effets délétères ni sur les paramètres de la reproduction ni sur la fertilité des mâles et des femelles. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
4.8. Interactions médicamenteuses et autres formes d'interactions
L’administration concomitante de ce produit avec des dépresseurs du système nerveux central (SNC) pourrait potentialiser les effets dépresseurs sur le SNC et l’appareil respiratoire.
Ce produit peut amplifier l’effet des médicaments qui abaissent le seuil épileptogène. Les médicaments ayant un effet inhibiteur (cimétidine et érythromycine, par exemple) ou inducteur (carbamazépine, par exemple) sur le métabolisme lié au cytochrome P450 peuvent influer sur l’effet analgésique de ce produit. L’importance clinique de cette interaction n’a pas encore été entièrement étudiée.
Il n’est pas conseillé d’associer ce produit à des mélanges d’agonistes / antagonistes (buprénorphine, butorphanol, par exemple), car l’effet analgésique d’un agoniste pur peut théoriquement être réduit dans de telles circonstances.
Voir la rubrique « Contre-indications ».
4.9. Posologie et voie d'administration
Voie orale.
La dose recommandée est de 2 à 4 mg de chlorhydrate de tramadol par kg de poids corporel toutes les 8 heures ou selon les besoins, en fonction de l’intensité de la douleur.
Les doses doivent être espacées de 6 heures au minimum. La dose quotidienne maximale recommandée est de 16 mg/kg. La réponse au tramadol étant variable selon l’individu et dépendant en partie de la posologie, de l’âge de l’animal, des différences individuelles de sensibilité à la douleur et de l’état général de l’animal, la posologie optimale devra être adaptée au cas par cas en s’appuyant sur les plages de doses et les fréquences de renouvellement indiquées ci-dessus. Le chien devra être examiné régulièrement par un vétérinaire pour déterminer si une analgésie supplémentaire est requise. L’analgésie supplémentaire pourra être obtenue en augmentant la dose de tramadol jusqu’à l’atteinte de la dose quotidienne maximale et/ou en adoptant une approche multimodale par ajout d’autres analgésiques adéquats.
A noter que le tableau posologique ci-dessous est donné à titre de guide pour l’administration du produit à la limite supérieure de la plage de doses : 4 mg/kg de poids corporel. Il indique le nombre de comprimés à administrer pour une dose de 4 mg de chlorhydrate de tramadol par kg de poids corporel.

Les comprimés peuvent être divisés en 2 ou 4 parties égales pour assurer le dosage précis. Placer le comprimé sur une surface plane, la face portant la barre de sécabilité étant tournée vers le haut et la face convexe (arrondie) vers la surface.
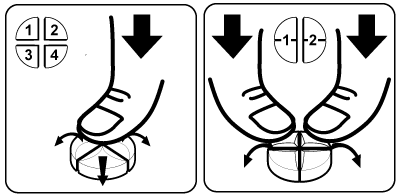
Division en 4 parties égales : appuyer avec le pouce au centre du comprimé.
Division en 2 parties égales : appuyer avec les pouces sur les deux côtés du comprimé.
4.10. Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
En cas d’intoxication au tramadol, des symptômes similaires à ceux observés avec d’autres analgésiques à action centrale (opioïdes) sont susceptibles de se produire. Ils comprennent, en particulier, un myosis, des vomissements, un collapsus cardiovasculaire, des troubles de conscience pouvant aller jusqu’au coma, des convulsions et une dépression respiratoire pouvant aller jusqu’à l’arrêt respiratoire.
Mesures générales d’urgence : maintenir les voies respiratoires dégagées, assurer un soutien cardio-respiratoire selon les symptômes. Induire le vomissement afin de vider l’estomac est approprié, sauf si l’animal affecté montre un état de conscience réduit, auquel cas un lavage d’estomac peut être envisagé. L’antidote en cas de dépression respiratoire est la naloxone. Toutefois, la naloxone risque de ne pas être efficace dans tous les cas de surdosage car il se peut qu’elle n’inverse que partiellement certains des autres effets du tramadol. En cas de crises convulsives, administrer du diazépam.
4.11. Temps d'attente
Sans objet.
5. Propriétés pharmacologiques
Groupe pharmacothérapeutique : analgésiques, autres opioïdes, tramadol.
Code ATC-vet : QN02AX02
5.1. Propriétés pharmacodynamiques
Le tramadol est un analgésique à action centrale dont le mécanisme d’action est complexe, celui-ci étant exercé par ses 2 énantiomères et son métabolite primaire, en faisant intervenir les récepteurs aux opioïdes, à la noradrénaline et à la sérotonine. L’énantiomère (+) du tramadol fait preuve d’une faible affinité envers les récepteurs µ aux opioïdes, inhibe la capture de la sérotonine et amplifie sa libération. L’énantiomère (-) inhibe préférentiellement la recapture de la noradrénaline. Le métabolite O--déméthyltramadol (M1) dispose d’une plus forte affinité pour les récepteurs µ aux opioïdes.
Contrairement à la morphine, le tramadol est dépourvu d’effet dépresseur sur la respiration dans un large intervalle de doses analgésiques. De même, il n’a pas d’influence sur la motilité gastro-intestinale. Les effets sur le système cardiovasculaire ont tendance à être de faible intensité. La puissance analgésique du tramadol est d’environ 1/10ème à 1/6ème de celle de la morphine.
5.2. Caractéristiques pharmacocinétiques
Le tramadol est rapidement absorbé : après administration d’une dose orale unique de 4,2 mg de chlorhydrate de tramadol par kg de poids corporel, une concentration plasmatique maximale de 18,49 ng de tramadol par mL est atteinte en 1 heure environ. La nourriture n’a pas d’effet significatif sur l’absorption du médicament.
Le tramadol est métabolisé dans le foie par déméthylation via le cytochrome P450, puis par conjugaison avec l’acide glucuronique. Chez le chien, les taux de métabolite actif O-déméthyltramadol sont plus faibles que chez l’être humain. L’élimination se fait principalement par les reins, la demi-vie d’élimination étant d’environ 45 minutes.
6. Informations pharmaceutiques
6.1. Liste des excipients
Cellulose microcristalline
Amidon prégélatinisé
Arôme boeuf
Saccharine sodique
Silice colloïdale anhydre
Stéarate de magnésium
Arôme masquant
6.2. Incompatibilités majeures
Sans objet.
6.3. Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
6.4. Précautions particulières de conservation
Après avoir perforé une alvéole, remettre les parties de comprimé inutilisées dans l’alvéole et replacer dans la boîte en carton.
Pas de précautions particulières de conservation.
6.5. Nature et composition du conditionnement primaire
Plaquette thermoformée PVC-PVDC / aluminium thermoscellée
6.6. Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
7. Titulaire de l'autorisation de mise sur le marché
DOMES PHARMA
3 RUE ANDRE CITROEN
63430 PONT DU CHATEAU
FRANCE
8. Numéro(s) d'autorisation de mise sur le marché
FR/V/4370380 3/2022
Boîte de 1 plaquette thermoformée de 10 comprimés quadrisécables
Boîte de 3 plaquettes thermoformées de 10 comprimés quadrisécables
Boîte de 6 plaquettes thermoformées de 10 comprimés quadrisécables
Boîte de 10 plaquettes thermoformées de 10 comprimés quadrisécables
Toutes les présentations peuvent ne pas être commercialisées.
9. Date de première autorisation/renouvellement de l'autorisation
03/02/2022
10. Date de mise à jour du texte
03/02/2022