TRAMATAB M COMPRIMES A CROQUER POUR CHIENS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un comprimé contient : |
|
|
|
Substance(s) active(s) : |
|
Tramadol (sous forme de chlorhydrate) ……………….. | 43,9 mg |
Équivalant à 50 mg de chlorhydrate de tramadol | |
Excipient(s) :
Composition qualitative en excipients et autres composants |
Lactose monohydraté |
Cellulose microcristalline (E460) |
Carboxyméthylamidon sodique type A |
Silice colloïdale hydratée |
Stéarate de magnésium |
Arôme poulet |
Comprimé brun clair avec des taches brunes, de forme ronde et convexe, avec une ligne de rupture en forme de croix sur un côté. Le comprimé peut être divisé en 2 ou 4 parties égales.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens.
3.2 Indications d'utilisation pour chaque espèce cible
Réduction des douleurs aiguës et chroniques légères des tissus mous et de l'appareil locomoteur.
3.3 Contre-indications
Ne pas administrer en même temps que des antidépresseurs tricycliques, des inhibiteurs de la monoamine oxydase et des inhibiteurs de la recapture de la sérotonine.
Ne pas utiliser en cas d'hypersensibilité au tramadol ou à l'un des excipients.
Ne pas utiliser chez les animaux épileptiques.
3.4 Mises en garde particulières
Les effets analgésiques du chlorhydrate de tramadol peuvent être variables. Il est envisagé que cela soit dû à des différences individuelles dans le métabolisme du médicament en O-desméthyltramadol, le principal métabolite actif. Chez certains chiens (non répondeurs), cela peut avoir pour conséquence que le médicament vétérinaire n'apporte pas d'analgésie. En cas de douleur chronique, une analgésie multimodale doit être envisagée. Les chiens doivent être suivis régulièrement par un vétérinaire afin de garantir un soulagement adéquat de la douleur. En cas de récurrence de la douleur ou d'analgésie insuffisante, il peut être nécessaire de reconsidérer le protocole analgésique.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Les comprimés étant aromatisés, les conserver hors de portée des animaux afin d'éviter toute ingestion accidentelle.
Utiliser avec prudence chez les chiens présentant une insuffisance rénale ou hépatique. Chez les chiens présentant une insuffisance hépatique, le métabolisme du tramadol en métabolites actifs peut être diminué, ce qui peut réduire l'efficacité du médicament vétérinaire. L'un des métabolites actifs du tramadol est excrété par voie rénale. Il peut dès lors s’avérer nécessaire d’adapter le schéma posologique utilisé chez les chiens souffrant d'insuffisance rénale. Les fonctions rénales et hépatiques doivent être surveillées lors de l'utilisation de ce médicament vétérinaire. L'arrêt d'un traitement analgésique à long terme doit être progressif dans la mesure du possible.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le tramadol peut provoquer des réactions d'hypersensibilité. Les personnes souffrant d'une hypersensibilité au tramadol doivent éviter tout contact avec le produit vétérinaire. Lavez-vous les mains après utilisation. Consultez un médecin en cas de réactions d'hypersensibilité.
Le tramadol peut provoquer une irritation des yeux, par exemple en cas de formation de poussière lors de la fragmentation des comprimés. Évitez le contact avec les yeux, y compris le contact main-œil. En cas de contact du médicament vétérinaire avec les yeux, rincez immédiatement et abondamment avec de l'eau.
Le tramadol peut provoquer une sédation, des nausées et des vertiges en cas d'ingestion accidentelle. Pour éviter toute ingestion accidentelle, en particulier par un enfant, les comprimés non utilisés doivent être replacés dans la plaquette ouverte, réinsérés dans la boîte et conservés dans un endroit sûr, hors de la vue et de la portée des enfants.
En cas d'ingestion accidentelle, en particulier par des enfants, consultez immédiatement un médecin et montrez-lui la notice ou l’étiquette. En cas d'ingestion accidentelle par des adultes : NE CONDUISEZ-PAS en raison du risque de somnolence.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens :
Fréquent (1 à 10 animaux / 100 animaux traités) : | Sédation1,2, Somnolence - trouble neurologique2 |
Peu fréquent (1 à 10 animaux / 1 000 animaux traités) : | Nausées, Vomissements |
Rare (1 à 10 animaux / 10 000 animaux traités) : | Hypersensitibilité3 |
Très rare ( < 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Convulsions4 |
1: léger.
2: surtout en cas d'administration de doses plus élevées.
3: en cas de réactions d'hypersensibilité, le traitement doit être interrompu.
4: chez les chiens dont le seuil de crise est bas.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la rubrique « coordonnées » de la notice.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
Gestation et lactation :
Les études de laboratoire sur les souris et/ou les rats et les lapins n'ont pas mis en évidence d'effets tératogènes, fœtotoxiques, maternotoxiques ni d'effets néfastes sur le développement péri- et postnatal de la progéniture.
Fertilité :
Les études de laboratoire sur les souris et/ou les rats et les lapins, avec le tramadol à des doses thérapeutiques, n'ont pas induit l'apparition de réactions défavorables sur les paramètres de reproduction et la fertilité chez le mâle et la femelle.
3.8 Interactions médicamenteuses et autres formes d'interactions
L'administration concomitante du médicament vétérinaire avec des dépresseurs du système nerveux central peut potentialiser les effets dépresseurs sur le SNC et la respiration. Le tramadol peut augmenter l'effet des médicaments qui abaissent le seuil des crises d'épilepsie.
Les substances qui inhibent (par exemple la cimétidine et l'érythromycine) ou induisent (par exemple la carbamazépine) le métabolisme médié par le CYP450 peuvent avoir un effet sur l'effet analgésique du tramadol. La pertinence clinique de ces interactions n'a pas été étudiée chez les chiens.
La combinaison d'agonistes/antagonistes mixtes (par exemple buprénorphine, butorphanol) et de tramadol n'est pas conseillée, car l'effet analgésique d'un agoniste pur peut être théoriquement réduit en pareilles circonstances.
Voir également la rubrique 3.3.
3.9 Voies d'administration et posologie
Voie orale.
La dose recommandée est de 2-4 mg de chlorhydrate de tramadol par kg de poids corporel toutes les 8 heures ou au besoin en fonction de l'intensité de la douleur.
L'intervalle minimal entre les doses est de 6 heures. La dose journalière maximale recommandée est de 16 mg/kg. La réponse individuelle au tramadol étant variable et dépendant en partie du dosage, de l'âge du patient, des différences individuelles de sensibilité à la douleur et de l'état général, le schéma posologique optimal doit être adapté à chaque individu en utilisant les fourchettes de doses et d'intervalles de retraitement ci-dessus. Le chien doit être examiné régulièrement par un vétérinaire afin de déterminer si une analgésie supplémentaire est nécessaire par la suite. Une analgésie supplémentaire peut être administrée en augmentant la dose de tramadol jusqu'à ce que la dose quotidienne maximale soit atteinte, et/ou en suivant une approche analgésique multimodale avec l'ajout d'autres analgésiques appropriés.
Il convient d'utiliser les dosages de comprimés les plus appropriés afin d'obtenir des taux de dosage précis et de minimiser les comprimés divisés à conserver jusqu'à la prochaine prise. La ou les fractions restantes de comprimé doivent être utilisées lors de la ou des prochaines administrations.
Pour garantir un dosage correct, le poids corporel doit être déterminé aussi précisément que possible.
Veuillez noter que ce tableau de dosage est destiné à servir de guide pour la délivrance du médicament vétérinaire à l'extrémité supérieure de la plage de doses : 4 mg/kg de poids corporel. Il indique le nombre de comprimés nécessaires pour administrer 4 mg de chlorhydrate de tramadol par kg de poids corporel et par administration. La dose recommandée est de 2-4 mg de chlorhydrate de tramadol par kg de poids corporel. Ce tableau donne un exemple de 4 mg de chlorhydrate de tramadol par kg de poids corporel.
Poids corporel (kg) | Nombre de comprimés de 50 mg |
6,25 | ½ |
12,5 | 1 |
18,75 | 1½ |
25 | 2 |
31,25 | 2½ |
37,5 | 3 |
50 | 4 |
Les comprimés peuvent être divisés en 2 ou 4 parties égales pour garantir un dosage précis. Pour ce faire, placer le comprimé sur une surface plane, face rainurée vers le haut et côté convexe (arrondi) contre la surface.
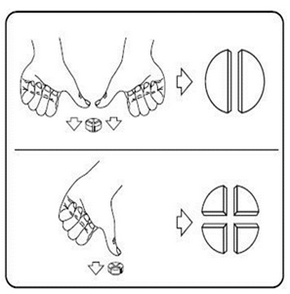
Moitiés : exercer une pression sur les deux côtés du comprimé avec les pouces.
Quartiers : exercer une pression au centre du comprimé avec le pouce.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
En cas d'intoxication au tramadol, des symptômes similaires à ceux observés avec d'autres analgésiques à action centrale (opioïdes) sont susceptibles de se produire. Il s'agit en particulier de myosis, de vomissements, de collapsus cardiovasculaire, de troubles de la conscience pouvant aller jusqu'au coma, de convulsions et de dépression respiratoire pouvant aller jusqu'à l'arrêt respiratoire.
Mesures générales d'urgence : Maintenir les voies respiratoires libres, soutenir les fonctions cardiaques et respiratoires en fonction des symptômes. Provoquer des vomissements pour vider l'estomac est approprié, sauf si l'animal atteint présente une perte de conscience, auquel cas un lavage gastrique peut être envisagé. L'antidote pour la dépression respiratoire est la naloxone. Cependant, la naloxone peut ne pas être utile dans tous les cas de surdosage au tramadol, car elle ne peut inverser que partiellement certains des autres effets du tramadol. En cas de convulsions, administrer du diazépam.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QN02AX02.
4.2 Propriétés pharmacodynamiques
Le tramadol est un analgésique à action centrale avec un mode d'action complexe, exercé par ses 2 énantiomères et son métabolite primaire, impliquant les récepteurs opioïdes, de norépinéphrine et de sérotonine. L'énantiomère (+) du tramadol a une faible affinité pour les récepteurs μ-opioïdes, il inhibe la recapture de la sérotonine et augmente sa libération. L'énantiomère (-) inhibe de préférence la recapture de la norépinéphrine. Le métabolite O-desméthyltramadol (M1) présente une plus grande affinité pour les récepteurs μ-opioïdes.
Contrairement à la morphine, le tramadol n'a pas d'effets dépressifs sur la respiration pour une gamme étendue de doses analgésiques. De même, il n'affecte pas la motilité gastro-intestinale. Les effets sur le système cardiovasculaire sont généralement légers. Le pouvoir analgésique du tramadol représente environ 1/10 à 1/6 de celui de la morphine.
4.3 Propriétés pharmacocinétiques
Le tramadol est facilement absorbé : Après une administration orale unique de 4 mg de tramadol HCL par kg de poids corporel, les concentrations plasmatiques maximales de 115 ng de tramadol par ml sont atteintes au bout de 40 minutes. Les aliments n'affectent pas de manière significative l'absorption du médicament.
Le tramadol est métabolisé dans le foie par déméthylation médiée par le cytochrome P450, suivie d'une conjugaison avec l'acide glucuronique. Chez les chiens, les niveaux de formation du métabolite actif O-desméthyltramadol sont plus faibles que chez l'homme. L'élimination se fait principalement par les reins, avec une demi-vie d'élimination d'environ 0,5-2 heures.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
5.3 Précautions particulières de conservation
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
5.4 Nature et composition du conditionnement primaire
Plaquettes en aluminium-PVC/aluminium/oPA, contenant 10 comprimés.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
CP-PHARMA HANDELSGESELLSCHAFT MBH
OSTLANDRING 13
31303 BURGDORF
ALLEMAGNE
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/0183318 6/2024
Boîte en carton de 10 comprimés
Boîte en carton de 30 comprimés
Boîte en carton de 50 comprimés
Boîte en carton de 100 comprimés
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
21/02/2024
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
21/02/2024
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments https://medicines.health.europa.eu/veterinary.