AMOXIBACTIN 500 MG COMPRIMES POUR CHIENS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé contient : |
|
|
|
Substance active : |
|
Amoxicilline ……………………………….…...….. | 500 mg |
(sous forme de trihydrate) |
|
(équivalant à 575 mg de trihydrate d’amoxicilline) |
|
|
|
Excipients : |
|
Stéarate de magnésium |
Silice colloïdale anhydre |
Carboxyméthylamidon sodique (type A) |
Lactose monohydraté |
Levure (déshydratée) |
Arôme poulet |
Comprimé blanc à blanc cassé tacheté de brun, rond et convexe, aromatisé, avec une barre de sécabilité en croix sur une face.
Les comprimés peuvent être divisés en deux ou quatre parties égales.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens.
3.2 Indications d'utilisation pour chaque espèce cible
Traitement des infections primaires et secondaires des voies respiratoires, telles que la rhinite due à pasteurella spp. et Streptococcus spp., et la bronchopneumonie due à Pasteurella spp., Escherichia coli et aux cocci à Gram positif.
Traitement des infections primaires des voies urogénitales, telles que la pyélonéphrite et les infections urinaires basses dues à Escherichia coli, Proteus spp. et aux cocci à Gram positif, l'endométrite due à Escherichia coli, Streptococcus canis et Proteus spp., et la vaginite consécutive à des infections mixtes.
Traitement des infections des glandes mammaires dues aux cocci à Gram positif et à Escherichia coli.
Traitement des infections cutanées localisées dues à Streptococcus spp.
3.3 Contre-indications
Ne pas utiliser en cas d'hypersensibilité aux pénicillines ou à d'autres substances de la famille des ß-lactamines ou à l'un des excipients.
Ne pas administrer aux gerbilles, cobayes, hamsters, lapins et chinchillas.
Ne pas utiliser chez les animaux présentant un dysfonctionnement rénal grave accompagné d'anurie ou d'oligurie.
3.4 Mises en garde particulières
Aucune.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Chez les animaux présentant un dysfonctionnement hépatique et rénal, le schéma posologique doit être soigneusement évalué et l'utilisation du médicament vétérinaire doit reposer sur une évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
Une prudence particulière est conseillée en cas d'utilisation chez de petits herbivores autres que ceux mentionnés dans la rubrique 3.3.
En raison de la probable variabilité (temporelle et géographique) de survenue des résistances bactériennes à l'amoxicilline, un échantillonnage bactériologique et un test de sensibilité sont recommandés. Une augmentation de la résistance a été rapportée chez des isolats d’E. coli incluant des E. coli multi-résistantes.
Des précautions spéciales doivent être prises en cas de suspicion de multi-résistance basée sur des tests de sensibilité.
Dans la mesure du possible, le médicament vétérinaire devra être utilisé uniquement sur la base d'un test de sensibilité.
L'utilisation du médicament vétérinaire en dehors des recommandations du RCP peut augmenter la prévalence des bactéries résistantes à l'amoxicilline et diminuer l'efficacité du traitement par d'autres antibiotiques de la famille des bêta-lactamines ou par d'autres classes d'antibiotiques en raison du risque de résistance croisée.
L’utilisation du médicament vétérinaire doit être conforme aux politiques officielles, nationales et régionales concernant les antimicrobiens.
Les comprimés sont aromatisés. Afin d'éviter toute ingestion accidentelle, tenir hors de la portée des animaux.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Les pénicillines et les céphalosporines peuvent provoquer une hypersensibilité (allergie) après injection, inhalation, ingestion ou contact cutané. L'hypersensibilité aux pénicillines peut entraîner des réactions croisées aux céphalosporines et inversement. Les réactions allergiques à ces substances peuvent occasionnellement être graves.
Ne manipulez pas ce médicament vétérinaire si vous savez y être sensibilisé(e) ou s'il vous a été conseillé de ne pas travailler avec ce type de préparations.
Manipulez ce médicament vétérinaire avec un soin extrême afin d'éviter toute exposition, en prenant toutes les précautions recommandées.
Si vous développez des symptômes après exposition, tels qu'une éruption cutanée, consultez un médecin et montrez-lui cette mise en garde. Le gonflement du visage, des lèvres ou des yeux ou les difficultés à respirer constituent des symptômes plus graves et nécessitent une prise en charge médicale urgente.
Lavez-vous les mains après avoir manipulé les comprimés.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens :
Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Vomissements a, diarrhée a Réaction d’hypersensibilité (réaction allergique cutanée, anaphylaxie) b |
a Légers.
b Dans ce cas, interrompre l’administration et administrer un traitement symptomatique.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation et de lactation.
Gestation et lactation :
Les études de laboratoire sur des rats n’ont pas mis en évidence d’effets tératogènes, fœtotoxiques ou maternotoxiques. L’utilisation ne doit se faire qu'après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
3.8 Interactions médicamenteuses et autres formes d'interactions
Le chloramphénicol, les macrolides, les sulfamides et les tétracyclines peuvent inhiber l'effet antibactérien des pénicillines en raison de l'apparition rapide de leur action bactériostatique. Le risque de réaction allergique croisée avec d'autres pénicillines doit être pris en compte.
Les pénicillines peuvent amplifier les effets des aminosides.
3.9 Voies d'administration et posologie
Voie orale.
Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible.
La dose recommandée est de 10 mg d'amoxicilline par kg de poids corporel, deux fois par jour pendant un minimum de 5 jours consécutifs. Dans la majorité des cas courants, l'infection répond à un traitement de 5 à 7 jours. Si aucune amélioration n'est observée après 5 à 7 jours, le diagnostic doit être réévalué. En cas d'infection chronique ou réfractaire, un traitement plus long peut être nécessaire.
Le tableau ci-dessous indique les quantités de médicament vétérinaire à administrer à la dose standard de 10 mg par kg de poids corporel deux fois par jour.

Les comprimés peuvent être divisés en deux ou quatre parties égales pour s'assurer d'une posologie exacte. Placez le comprimé sur une surface plate, avec la face portant la barre de sécabilité tournée vers le haut et la face convexe (arrondie) tournée vers le plan de travail.
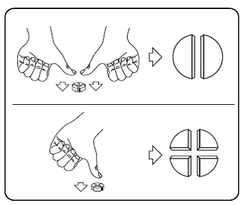
Deux demi-comprimés : appuyez avec vos pouces des deux côtés du comprimé.
Quatre quarts de comprimé : appuyez avec votre pouce au centre du comprimé.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
En cas surdosage, aucun effet indésirable autre que ceux décrits dans la rubrique 3.6 n'a été identifié.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QJ01CA04.
4.2 Propriétés pharmacodynamiques
Propriétés générales
L'amoxicilline est un antibiotique de la famille des bêta-lactamines et sa structure comprend le cycle bêta-lactame et le cycle thiazolidine communs à toutes les pénicillines. Les antibiotiques de la famille des bêta-lactamines empêchent la formation de la paroi cellulaire bactérienne en interférant avec la phase finale de la synthèse du peptidoglycane. Ils inhibent l'activité des enzymes transpeptidases, qui catalysent la réticulation des polymères de glycopeptides formant la paroi cellulaire. Ils exercent une action bactéricide mais provoquent uniquement la lyse des cellules en cours de croissance. Les antibiotiques de la famille des bêta-lactamines peuvent être désignés sous l'appellation d'antibiotiques temps-dépendants.
Spectre antibiotique
L'amoxicilline est un antibiotique à large spectre, généralement actif contre certaines bactéries à Gram négatif et contre la plupart des bactéries à Gram positif (Germ-vet 2007), p. ex. les germes sensibles à la pénicilline de type Pasteurella spp., Proteus spp., Streptococcus spp., E. coli et cocci à Gram positif.
Résistance
L'amoxicilline est acido-résistante mais n'est pas résistante à l'action des bêta-lactamases, qui peuvent hydrolyser les molécules, entraînant l'ouverture de la structure du cycle bêta-lactame et l'inactivation de l'antibiotique.
La plupart des bactéries à Gram négatif présentent une résistance intrinsèque à de nombreuses bêta-lactamines. Cela est dû en partie au mécanisme d'action du médicament et à la structure de la membrane bactérienne.
La résistance acquise aux bêta-lactamines au sein des isolats cliniques peut être due à l'activité des bêta-lactamases induite par les plasmides ou à des mutations affectant les locus chromosomiques. Dans certaines souches, une mutation unique peut être responsable d'une résistance tandis que, dans d'autres souches, la résistance peut être due à plusieurs mutations.
La prévalence de la résistance acquise peut être élevée avec E. coli.
4.3 Propriétés pharmacocinétiques
L'amoxicilline est bien absorbée après administration orale. Chez le chien, la biodisponibilité systémique est de 60-70 %. L'amoxicilline présente un volume de distribution apparent relativement faible, un faible taux de liaison avec les protéines plasmatiques (34 % chez le chien) et une demi-vie d'élimination brève en raison de l'excrétion tubulaire active par les reins.
Après absorption, les concentrations les plus élevées sont constatées dans les reins (urine) et la bile, suivis du foie, des poumons, du cœur et de la rate.
La diffusion de l'amoxicilline dans le liquide céphalo-rachidien est faible, sauf en cas d'inflammation des méninges.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
Durée de conservation des comprimés divisés : 4 jours.
5.3 Précautions particulières de conservation
À conserver à une température ne dépassant pas 30°C.
Toute fraction de comprimé non utilisée doit être replacée dans la plaquette.
5.4 Nature et composition du conditionnement primaire
Plaquette thermoformée polychlorure de vinyle / polyéthylène / chlorure de polyvinylidene – aluminium.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
LE VET. BEHEER B.V.
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/0807194 3/2014
Boîte de 1 plaquette thermoformée de 10 comprimés sécables
Boîte de 2 plaquettes thermoformées de 10 comprimés sécables
Boîte de 3 plaquettes thermoformées de 10 comprimés sécables
Boîte de 4 plaquettes thermoformées de 10 comprimés sécables
Boîte de 5 plaquettes thermoformées de 10 comprimés sécables
Boîte de 6 plaquettes thermoformées de 10 comprimés sécables
Boîte de 7 plaquettes thermoformées de 10 comprimés sécables
Boîte de 8 plaquettes thermoformées de 10 comprimés sécables
Boîte de 9 plaquettes thermoformées de 10 comprimés sécables
Boîte de 10 plaquettes thermoformées de 10 comprimés sécables
Boîte de 25 plaquettes thermoformées de 10 comprimés sécables
Boîte de 50 plaquettes thermoformées de 10 comprimés sécables
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
06/10/2014
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
07/05/2026
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).