ARENTOR DC 250 MG SUSPENSION INTRAMAMMAIRE POUR VACHES TARIES
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque seringue pour administration intramammaire de 3 g contient : | |
|
|
Substance(s) active(s) : |
|
Céfalonium | 250 mg |
(sous forme de dihydrate) |
|
Composition qualitative en excipients et autres composants |
Distéarate d’aluminium |
Paraffine liquide |
Suspension de couleur crème jaune pâle
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Bovins (vaches taries).
3.2 Indications d'utilisation pour chaque espèce cible
Traitement des mammites subcliniques au tarissement causées par Staphylococcus aureus, Streptococcus agalactiae, Streptococcus dysgalactiae, Streptococcus uberis, Trueperella pyogenes, Escherichia coli et Klebsiella spp., sensibles au céfalonium.
3.3 Contre-indications
Ne pas utiliser en cas d’hypersensibilité aux céphalosporines, à d'autres antibiotiques de la classe des bêta-lactamines ou à l’un des excipients.
3.4 Mises en garde particulières
Aucune.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
L’utilisation du médicament vétérinaire doit être basée sur l’identification et des tests de sensibilité des agents pathogènes cibles. Si cela n’est pas possible, le traitement doit être fondé sur des informations épidémiologiques et sur les connaissances relatives à la sensibilité des agents pathogènes cibles au niveau de l’exploitation ou au niveau local/régional.
L'utilisation du médicament vétérinaire doit être conforme aux politiques antimicrobiennes officielles, nationales et régionales.
Un antibiotique présentant un risque moindre de sélection de résistances aux antibiotiques (antibiotique de catégorie AMEG inférieure) doit être utilisé pour le traitement de première intention lorsque les tests de sensibilité suggèrent l'efficacité probable de cette approche.
L’utilisation du médicament vétérinaire en dehors des recommandations du RCP peut augmenter la prévalence des bactéries résistantes au céfalonium et peut diminuer l’efficacité du traitement avec d’autres antibiotiques bêta-lactamines.
Les protocoles thérapeutiques utilisés chez les vaches en période sèche doivent prendre en compte les politiques locales et nationales d’utilisation des antibiotiques et doivent être périodiquement réexaminés par un vétérinaire.
Il convient d'éviter que les veaux soient nourris avec du lait contenant des résidus de céfalonium jusqu’à la fin du temps d’attente fixé pour le lait, excepté pendant la phase colostrale car cela pourrait conduire à la sélection de bactéries résistantes aux antibiotiques dans le microbiote intestinal du veau et augmenter l’excrétion fécale de ces bactéries.
L’efficacité du médicament vétérinaire n’a été établie que pour les pathogènes mentionnés dans la rubrique 3.2 « Indications d'utilisation pour chaque espèce cible ». Par conséquent, une mammite aigue grave (pouvant être mortelle) due à d'autres germes pathogènes, en particulier Pseudomonas aeruginosa, peut survenir à la suite du tarissement. Pour diminuer ce risque, des règles d'hygiène strictes doivent être scrupuleusement respectées.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Les pénicillines et les céphalosporines peuvent provoquer des réactions d’hypersensibilité (allergie) après une injection, une inhalation, une ingestion ou un contact cutané. L’hypersensibilité aux pénicillines peut entraîner des réactions croisées avec les céphalosporines et inversement. Les réactions allergiques à ces substances peuvent parfois être graves.
Ne pas manipuler ce médicament vétérinaire en cas d’allergie ou s’il vous a été conseillé de ne pas entrer en contact avec ce type de molécules.
Manipuler ce médicament vétérinaire avec précautions pour éviter toute exposition et suivre les précautions recommandées.
En cas d’apparition, après l’exposition, de symptômes tels qu’une éruption cutanée, demandez conseil à un médecin et montrez-lui la notice ou l’étiquette. Un œdème du visage, des lèvres ou des yeux ou des difficultés respiratoires sont des symptômes plus graves qui nécessitent une consultation médicale d’urgence.
Se laver les mains après utilisation.
Les lingettes nettoyantes fournies avec le médicament vétérinaire intramammaire contiennent de l’alcool isopropylique. Porter des gants de protection en cas d’irritation cutanée connue ou suspecté due à l’alcool isopropylique. Éviter tout contact avec les yeux, car l’alcool isopropylique peut provoquer une irritation oculaire.
Précautions particulières concernant la protection de l'environnement
Autres précautions
Sans objet.
3.6 Effets indésirables
Très rare ( < 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Réactions d’hypersensibilité (agitation, tremblement, œdème de la mamelle, des paupières et des lèvres)1 |
1 Réactions immédiates décrites chez certains animaux, pouvant entraîner la mort de l’animal.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la rubrique « coordonnées » de la notice.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation :
Le médicament vétérinaire est destiné à être utilisé au cours du dernier trimestre de gestation, une fois la vache tarie. Le traitement n’engendre pas d’effet indésirable sur le fœtus.
Lactation :
Le médicament vétérinaire ne doit pas être utilisé chez les vaches pendant la lactation.
3.8 Interactions médicamenteuses et autres formes d'interactions
Les céphalosporines ne doivent pas être administrées simultanément avec des antibiotiques bactériostatiques. L’utilisation concomitante de céphalosporines et de médicaments néphrotoxiques peut augmenter la toxicité rénale.
3.9 Voies d'administration et posologie
Voie intramammaire.
La seringue pour l’administration intramammaire est à usage unique.
Administrer le contenu d’une seringue dans le canal du trayon de chaque quartier, immédiatement après la dernière traite. Ne pas plier l’embout. Après avoir retiré le capuchon, éviter toute contamination de l’embout. Avant administration du produit, nettoyer et désinfecter soigneusement le trayon (p. ex. avec les lingettes nettoyantes fournies).
Option 1 : pour une administration intramammaire avec l’embout court.
Tenir le corps de la seringue pour administration intramammaire et la base du capuchon d‘une main et tordre la petite partie haute du capuchon au-dessus du repère (la partie basse du capuchon restant fixée à la seringue). Veiller à ne pas contaminer l'embout.
Option 2 : pour une administration intramammaire avec l’embout complet.
Retirer le capuchon intégralement en tenant fermement le corps de la seringue d’une main, et avec le pouce, faire glisser le capuchon vers le haut jusqu’à ce qu’il se détache avec un déclic. Veiller à ne pas contaminer l'embout.
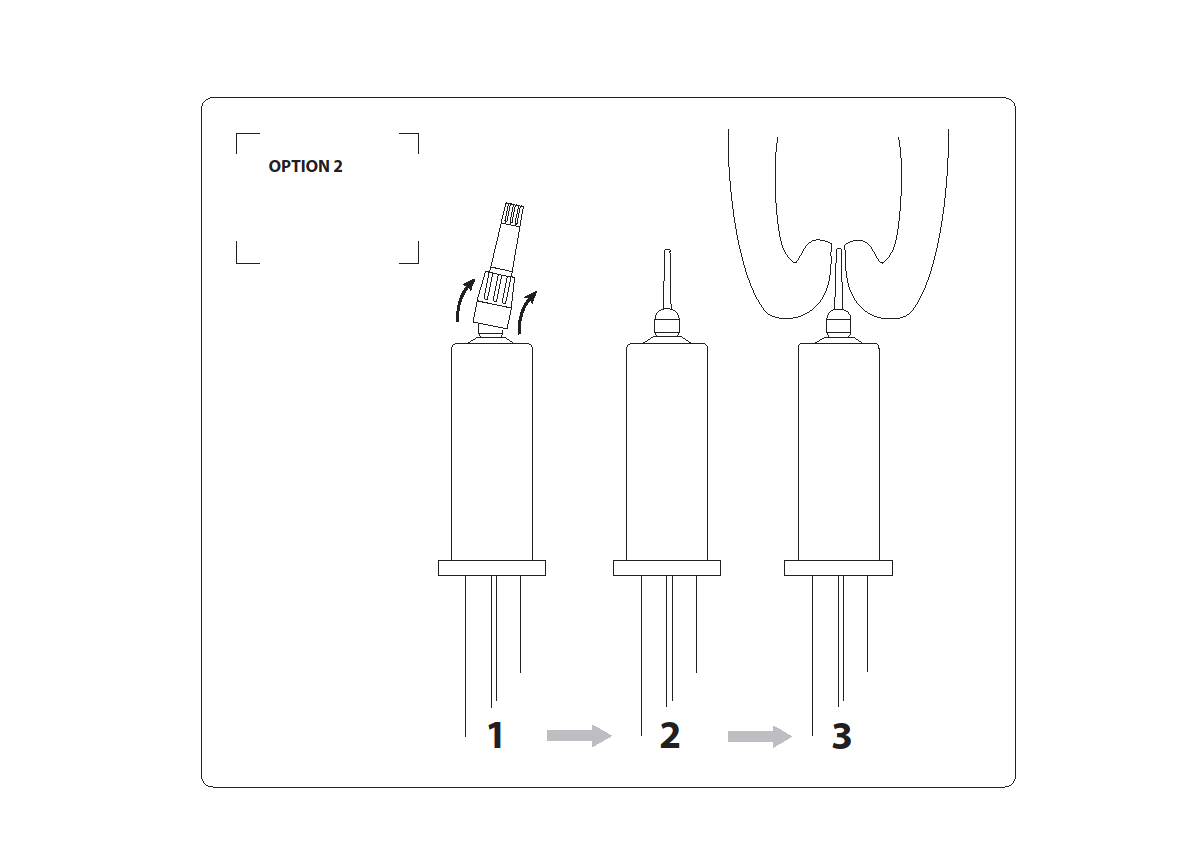
Insérer l’embout dans le canal du trayon et appliquer une pression constante sur le piston de la seringue pour administration intramammaire jusqu’à ce que toute la dose ait été délivrée. Maintenir l’extrémité du trayon avec une main et masser doucement vers le haut avec l'autre main afin de faciliter la diffusion de l'antibiotique dans le quartier.
Après administration, il est recommandé de procéder ensuite à un trempage des trayons dans une solution désinfectante spécifiquement destinée à cet usage.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
L'administration de doses répétées à des bovins pendant trois jours consécutifs n’a pas mis en évidence, ni induit d'effets indésirables.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Viande et abats : 21 jours.
Lait : 96 heures après le vêlage si la période de tarissement est supérieure à 54 jours.
58 jours après le traitement si la période de tarissement est inférieure ou égale à 54 jours.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QJ51DB90
4.2 Propriétés pharmacodynamiques
Le céfalonium est un antibiotique appartenant à la classe des céphalosporines de première génération, qui agit en inhibant la synthèse de la paroi cellulaire bactérienne (action bactéricide). L’activité antibactérienne n'est pas altérée en présence de lait.
Il existe trois mécanismes connus de résistance aux céphalosporines : perméabilité réduite de la paroi bactérienne, inactivation enzymatique et absence de sites de liaison spécifiques à la pénicilline. Chez les bactéries Gram positif, en particulier chez les staphylocoques, le principal mécanisme de résistance aux céphalosporines est l'altération des protéines de liaison à la pénicilline. Chez les bactéries Gram négatif, la résistance peut passer par la production de β-lactamases (à spectre large ou élargi).
Le céfalonium est actif contre Staphylococcus aureus, Streptococcus agalactiae, Streptococcus dysgalactiae, Streptococcus uberis, Trueperella pyogenes, Escherichia coli et Klebsiella spp., sensibles au céfalonium.
4.3 Propriétés pharmacocinétiques
Le céfalonium est largement mais lentement absorbé dans la mamelle et est principalement excrété dans l’urine. Entre 7 et 13 % de la substance active est éliminée dans l’urine chacun des trois premiers jours suivant l'administration, alors que, sur la même période, l’excrétion quotidienne dans les fèces est inférieure à 1 %.
Les concentrations sanguines moyennes restent relativement constantes pendant environ 10 jours après l’administration, ce qui est cohérent avec une absorption lente mais prolongée du céfalonium à partir de la mamelle.
La persistance à long terme du céfalonium dans la mamelle tarie a été étudiée sur une période de 10 semaines après l'administration. Des concentrations efficaces de céfalonium restaient présentes dans les sécrétions de la mamelle sur une période de 10 semaines après l’administration.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 2 ans.
5.3 Précautions particulières de conservation
À conserver à une température ne dépassant pas 25°C.
5.4 Nature et composition du conditionnement primaire
Seringue de 3 g pour administration intramammaire polyéthylène basse densité coloré avec un embout sécable enpolyéthylène basse densité coloré.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
UNIVET LIMITED
TULLYVIN
H16 T183 COOTEHILL (CO. CAVAN)
IRLANDE
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/0679381 0/2018
Boîte en carton de 20 seringues de 3 g pour administration intramammaire et de 20 lingettes nettoyantes imprégnées d’alcool isopropylique conditionnées individuellement.
Seau en plastique de 120 seringues de 3 g pour administration intramammaire et de 120 lingettes nettoyantes imprégnées d’alcool isopropylique conditionnées individuellement.
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
27/08/2018 - 28/01/2022
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
24/06/2024
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).