BIOCLINDAVET 275 MG COMPRIMES A CROQUER POUR CHIENS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé contient : |
|
|
|
Substance active : |
|
Clindamycine ……………………………………………. | 275 mg |
(sous forme de chlorhydrate) |
|
(équivalant à 298,62 mg de chlorhydrate de clindamycine) |
|
|
|
Excipients : |
Composition qualitative des excipients et autres composants |
Croscarmellose de sodium |
Cellulose microcristalline |
Lactose monohydraté |
Silice colloïdale hydratée |
Copovidone |
Arôme de viande |
Stéarate de magnésium |
Comprimé rond et convexe, blanc cassé tacheté de brun présentant une ligne de cassure en croix sur une face. Le comprimé peut être divisé en 2 ou 4 parts égales.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens.
3.2 Indications d'utilisation pour chaque espèce cible
- Traitement des plaies infectées, des abcès et des infections dentaires et de la cavité buccale causés par ou associés à des souches sensibles à la clindamycine de Staphylococcus spp, Streptococcus spp, Bacteroides spp, Fusobacterium necrophorum et Clostridium perfringens.
- Traitement de l’ostéomyélite causée par Staphylococcus aureus.
3.3 Contre-indications
Ne pas utiliser chez les hamsters, cobayes, lapins, chinchillas, chevaux ou ruminants, l’ingestion de clindamycine par ces espèces peut provoquer des troubles gastro-intestinaux sévères, pouvant entraîner la mort.
Ne pas utiliser en cas d’hypersensibilité à la clindamycine ou à la lincomycine, ou à l’un des excipients.
3.4 Mises en garde particulières
Une résistance croisée a été démontrée entre la clindamycine et différents antimicrobiens appartenant aux classes des lincosamides et des macrolides (dont l’érythromycine).
L’utilisation de la clindamycine doit être attentivement évaluée lorsque les antibiogrammes ont montré une résistance aux lincosamides et aux macrolides, car son efficacité peut être réduite.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
L’utilisation du médicament vétérinaire doit être basée sur l’identification et les tests de sensibilité du ou des agents pathogènes cibles, incluant le test de zone D.
Si cela n’est pas possible, le traitement doit être basé sur des informations épidémiologiques et la connaissance de la sensibilité des agents pathogènes cibles au niveau local/régional.
L’utilisation du médicament vétérinaire doit être conforme aux politiques officielles, nationales et régionales concernant les antimicrobiens.
Un antibiotique présentant un risque plus faible de selection de résistance aux antimicrobiens (catégorie AMEG inférieure) devrait être utilisé pour le traitement initial, lorsque les tests de sensibilité suggèrent l’efficacité probable de cette approche.
La clindamycine est susceptible de favoriser la prolifération de microorganismes non sensibles tels que les souches résistantes de Clostridia spp. et les levures. En cas de surinfection, des mesures correctrices appropriées doivent être prises en fonction de la situation clinique.
En cas d’administration de doses élevées de clindamycine ou lors de traitement prolongé d’un mois ou plus, des tests des fonctions hépatique et rénale ainsi que des numérations cellulaires doivent être réalisés périodiquement.
Chez les chiens présentant des problèmes rénaux et/ou hépatiques accompagnés de troubles sévères du métabolisme, la dose à administrer devra être déterminée avec précaution et leur état de santé devra être suivi en réalisant des tests sanguins appropriés pendant le traitement.
L’utilisation du médicament vétérinaire n’est pas recommandée chez les nouveau-nés.
Les comprimés sont aromatisés. Pour éviter toute ingestion accidentelle, conserver les comprimés hors de portée des animaux.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Lavez-vous soigneusement les mains après utilisation.
Ce médicament vétérinaire peut provoquer une hypersensibilité (réaction allergique). Les personnes présentant une hypersensibilité connue aux lincosamides (clindamycine et lincomycine) doivent éviter tout contact avec le médicament vétérinaire.
Des précautions doivent être prises pour éviter toute ingestion accidentelle, pouvant entraîner des effets gastro-intestinaux tels que douleur abdominale et diarrhée.
Pour éviter toute ingestion accidentelle, en particulier par un enfant, ne sortez les comprimés de la plaquette thermoformée qu’au moment de les administrer à l’animal. Replacer les parts de comprimé non utilisées dans l’alvéole de la plaquette, replacer celle-ci dans la boîte et conserver la boîte en lieu sûr, hors de la vue et de la portée des enfants.
En cas d’ingestion accidentelle, en particulier par un enfant, ou de réaction allergique, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Afin de limiter le risque lié aux résidus et aux bactéries résistantes, des précautions d’hygiène générales doivent être mises en œuvre. Le lavage des mains à l’eau et au savon est particulièrement recommandé lors de la manipulation des animaux traités, de leurs déchets et de leur litière.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens:
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) | Vomissement et/ou diarrhée |
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Des études à fortes doses chez le rat suggèrent que la clindamycine n’est pas tératogène et n’affecte pas significativement les performances de reproduction des mâles et des femelles.
L’innocuité du médicament vétérinaire chez les chiennes en gestation ou chez les chiens mâles reproducteurs n’a pas été établie.
L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
La clindamycine peut traverser la barrière placentaire et la barrière sang-lait. Par conséquent, le traitement des femelles allaitantes peut entraîner une diarrhée chez les chiots.
3.8 Interactions médicamenteuses et autres formes d'interactions
– Les sels d’aluminium et les hydroxydes, le kaolin et le complexe aluminium-magnésium-silicate peuvent réduire l’absorption gastro-intestinale des lincosamides. Les médicaments vétérinaires contenant ces substances doivent être administrés au moins 2 heures avant la clindamycine.
– Ciclosporine: la clindamycine peut réduire l’effet immunosuppresseur de la molécule avec un risque de manque d’efficacité.
– Bloquants neuromusculaires: la clindamycine possède une activité curarisante intrinsèque de blocage neuromusculaire et elle doit être utilisée avec précaution avec d’autres bloqueurs neuromusculaires (curares). La clindamycine peut accroître le blocage neuromusculaire.
– Ne pas utiliser la clindamycine en même temps que du chloramphénicol ou des macrolides, car ils ciblent la sous-unité 50S des ribosomes etdes effets antagonistes peuvent apparaître.
– En cas d’administration simultanée de clindamycine et d’aminoglycosides (p. ex. gentamicine), le risque d’interactions indésirables (insuffisance rénale aiguë) ne peut être exclu.
3.9 Voies d'administration et posologie
Voie orale.
Posologie recommandée:
-Plaies infectées, abcès et infections dentaires/de la cavité buccale: 11 mg de clindamycine par kg de poids corporel toutes les 24 heures pendant 28 jours au maximum. La durée du traitement est établie par le vétérinaire responsable.
-Traitement des infections osseuses (ostéomyélite): 11 mg de clindamycine par kg de poids corporel toutes les 12 heures pendant 28 jours au minimum. Le traitement doit être interrompu si aucun effet thérapeutique n’est observé au cours des 14 premiers jours.
Exemple:
– Pour une posologie de 11 mg/kg :
BIOCLINDAVET 275 mg | |
Poids (kg) | Nombre de comprimés par administration |
5-6,25 | ¼ de comprimé |
6,3-9,40 | Utiliser Bioclindavet 75 mg |
9,5-12,50 | ½ comprimé |
12,6-18,75 | ¾ de comprimé |
18,8-25,00 | 1 comprimé |
25,1-31,25 | 1 + ¼ de comprimé |
31,3-37,50 | 1 + ½ comprimé |
37,60-43,75 | 1 + ¾ de comprimé |
43,8-50,00 | 2 comprimés |
Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible.
Les comprimés peuvent être divisés en 2 ou 4 parts égales pour garantir une posologie appropriée.
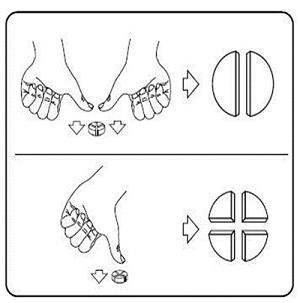
Placer le comprimé sur une surface plane, face portant la ligne de cassure vers le haut et face convexe (arrondie) sur la surface.
Moitiés : appuyer sur les deux côtés du comprimé avec les pouces.
Quarts : appuyer au centre du comprimé avec un pouce.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Aucun effet indésirable n’a été signalé chez les es chiens après administration d’une dose élevée de clindamycine allant jusqu’à 300 mg/kg. Des vomissements, une perte d’appétit, des diarrhées, une leucocytose et augmentation des enzymes hépatiques (ASAT/SGOT et ALAT/SGPT) ont été observés occasionnellement.
Des chiens recevant 600 mg/kg/j de clindamycine ont présenté anorexie, vomissement et perte de poids.
En cas de surdosage, arrêter immédiatement le traitement et mettre en place un traitement symptomatique.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QJ01FF01.
4.2 Propriétés pharmacodynamiques
La clindamycine est un antibiotique principalement bactériostatique appartenant au groupe des lincosamides. La clindamycine est un analogue chloré de la lincomycine. Elle agit en inhibant la synthèse des protéines bactériennes. Le couplage réversible à la sous-unité 50S du ribosome bactérien inhibe la traduction des acides aminés liés à l’ARNt, empêchant ainsi l’élongation de la chaîne peptidique.
Une résistance aux lincosamides seuls peut survenir, mais une résistance croisée avec les macrolides, les lincosamides et les streptogramines du groupe B (MLSB) est plus fréquente. La résistance résulte de la méthylation des résidus d’adénine sur l’ARN 23S de la sous-unité ribosomale 50S, ce qui empêche l’antibiotique de se lier au site cible. Différentes espèces bactériennes sont capables de synthétiser une enzyme codée par divers gènes erm (erythromycin ribosomal methylase) structurellement apparentés. Chez les bactéries pathogènes, ces gènes sont principalement présents dans des plasmides et des transposons (séquences capables de se déplacer de manière autonome). Les gènes erm prennent principalement la forme des variants erm(A) et erm(C) chez Staphylococcus aureus et du variant erm(B) chez Staphylococcus pseudintermedius, les streptocoques et les entérocoques. Les bactéries résistantes aux macrolides, initialement sensibles à la clindamycine, développent rapidement une résistance à la clindamycine en cas d’exposition aux macrolides. Ces bactéries posent un risque de sélection in vivo de mutants constitutifs.
Le CLSI fournit des valeurs seuils vétérinaires spécifiques à la clindamycine pour les infections de la peau et des tissus mous dues à Staphylococcus spp. et au groupe des streptocoques bêta-hémolytiques chez les chiens: S ≤ 0,5 μg/mL ; I = 1-2 μg/mL; R ≥ 4 μg/mL (CLSI, 2020).
La résistance de Staphylococcus spp. aux lincosamides semble être répandue en Europe, avec une moyenne arithmétique pondérée de résistance étant d’environ 25 % pour Staphylococcus pseudintermedius et Staphylococcus aureus (EFSA, 2021).
4.3 Propriétés pharmacocinétiques
La clindamycine est presque entièrement absorbée après administration orale.
À la suite d’une administration orale d’une dose de 11 mg/kg du médicament vétérinaire, une concentration plasmatique maximale de 5,7 µg/mL est atteinte en l’espace de 1 heure.
La clindamycine est largement distribuée et peut se concentrer dans certains tissus.
La demi-vie d’élimination moyenne de la clindamycine est de l’ordre de 6 heures.
La clindamycine est excrétée à approximativement 70 %dans les selles et 30 % dans les urines.
Environ 93 % de la clindamycine sont liés aux protéines plasmatiques.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
Durée de conservation après première ouverture du conditionnement primaire : 3 jours.
5.3 Précautions particulières de conservation
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
5.4 Nature et composition du conditionnement primaire
PVC/PE/PVDC (blanc) – Plaquettes en aluminium contenant chacune 10 comprimés.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
AXIENCE
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/6241488 5/2025
Boîte en carton de 10 comprimés (1 plaquette de 10 comprimés).
Boîte en carton de 30 comprimés (3 plaquettes de 10 comprimés).
Boîte en carton de 100 comprimés (10 plaquettes de 10 comprimés).
Boîte en carton de 250 comprimés (25 plaquettes de 10 comprimés).
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
17/11/2025
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
17/11/2025
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).