CYCLAVANCE 100 MG/ML SOLUTION BUVABLE POUR CHIENS ET CHATS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un mL contient : |
|
|
|
|
|
Substance(s) active(s) : |
|
|
Ciclosporine | 100 mg |
|
|
|
|
Excipient(s) : |
|
|
Composition qualitative en excipients et autres composants | Composition quantitative si cette information est essentielle à une bonne administration du médicament vétérinaire | |
Tout-rac-alpha-tocophérol (E 307) | 1,00 mg | |
Monolinoléate de glycérol | / | |
Ethanol anhydre (E 1510) | / | |
Hydroxystéarate de macrogolglycérol | / | |
Propylèneglycol (E 1520) | / | |
Solution claire à légèrement jaune.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens et chats.
3.2 Indications d'utilisation pour chaque espèce cible
Traitement des manifestations chroniques de la dermatite atopique chez les chiens.
Traitement symptomatique des dermatites allergiques chroniques chez les chats.
3.3 Contre-indications
Ne pas utiliser en cas d'hypersensibilité à la substance active ou à l'un des excipients.
Ne pas utiliser en cas d'antécédents d'affections malignes ou d'affections malignes évolutives.
Ne pas vacciner avec un vaccin vivant pendant le traitement ou pendant un intervalle de deux semaines avant ou après le traitement (voir les rubriques 3.5 « Précautions particulières d'emploi » et 3.8 « Interactions médicamenteuses et autres formes d’interactions »).
Ne pas utiliser chez les chiens de moins de 6 mois ou pesant moins de 2 kg.
Ne pas utiliser chez les chats infectés par le virus de la leucose féline (FeLV) ou le virus de l’immunodéficience féline (FIV).
3.4 Mises en garde particulières
L’utilisation d’autres mesures et/ou traitements pour contrôler le prurit modéré à sévère doit être envisagée lors de l’instauration d’un traitement par la ciclosporine.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Les signes cliniques de la dermatite atopique chez les chiens et de la dermatite allergique chez les chats comme le prurit et l’inflammation cutanée ne sont pas spécifiques à ces maladies ; de ce fait, les autres causes de dermatoses comme les infestations par les ectoparasites, les autres allergies responsables de signes dermatologiques (par exemple : allergie aux puces ou allergie alimentaire) ainsi que les infections bactériennes et fongiques doivent être écartées avant de démarrer le traitement. Il est souhaitable de traiter l’infestation par les puces avant et pendant le traitement de la dermatite atopique ou de la dermatite allergique.
Un examen clinique complet doit être réalisé avant le traitement. La ciclosporine n’induit pas de tumeur mais, inhibant l’activité des lymphocytes T, elle peut conduire à l’augmentation de l’incidence des manifestations cliniques d’affections malignes liée à la diminution de la réponse immunitaire antitumorale. L’augmentation potentielle du risque d’évolution d’une tumeur doit être prise en compte par rapport au bénéfice clinique. Si une lymphadénopathie est observée chez les animaux traités par la ciclosporine, d’autres examens cliniques sont recommandés et le traitement doit être interrompu si nécessaire.
Il est également recommandé d'éliminer toute infection bactérienne et fongique avant d'administrer le médicament. Par contre, l’apparition d’une infection en cours de traitement ne nécessite pas obligatoirement l’arrêt de ce dernier sauf si l’infection est sévère.
Chez l’animal de laboratoire, la ciclosporine est susceptible d’affecter les taux circulants d’insuline et d’entraîner une augmentation de la glycémie. Si des symptômes de diabète sucré sont observés suite à l’utilisation du produit, par exemple : polyurie, polydipsie, la dose doit être diminuée ou le traitement arrêté et un vétérinaire doit être consulté.
En présence de signes évocateurs de diabète sucré, l’effet du traitement sur la glycémie devra donc être surveillé. L’utilisation de la spécialité n’est pas recommandée chez les animaux diabétiques.
La vaccination doit faire l’objet d’une attention particulière. Le traitement avec le médicament vétérinaire peut modifier l’efficacité des vaccins. En cas de vaccins inactivés, il n’est pas recommandé de vacciner pendant le traitement ou dans l’intervalle de deux semaines avant ou après l’administration du médicament vétérinaire. Pour les vaccins vivants, voir la rubrique 3.3 « Contre-indications ».
Il n’est pas recommandé de traiter, de façon concomitante, avec un autre immunosuppresseur.
Chiens :
Surveiller la créatininémie chez les chiens souffrant d’insuffisance rénale sévère.
Chats :
La dermatite allergique chez le chat peut avoir diverses manifestations, y compris des plaques éosinophiliques, l’excoriation de la tête et du cou, une alopécie symétrique et / ou une dermatite miliaire.
Le statut immunitaire des chats vis-à-vis des infections aux FeLV et FIV doit être évalué avant le traitement.
Les chats qui sont séronégatifs pour T. gondii peuvent présenter un risque de développer une toxoplasmose clinique s’ils s’infectent au cours du traitement. Dans de rares cas, cela peut être fatal. L’exposition potentielle des chats séronégatifs ou des chats suspectés d’être séronégatifs à Toxoplasma doit donc être minimisée (par exemple, rester à l’intérieur, éviter la viande crue ou les restes de table). Cependant, dans une étude de laboratoire contrôlée, le traitement avec la ciclosporine n'a pas réactivé l'excrétion d'oocyste chez les chats préalablement exposés à T. gondii. En cas de toxoplasmose clinique ou d’autres maladies systémiques graves, arrêter le traitement par la ciclosporine et initier un traitement approprié.
Des études cliniques chez les chats ont montré qu’une baisse de l’appétit et une perte de poids peuvent survenir pendant le traitement par la ciclosporine. La surveillance du poids corporel est recommandée. Une réduction significative du poids corporel peut entraîner une lipidose hépatique. Si une perte de poids progressive et persistante se produit pendant le traitement, il est recommandé d’interrompre le traitement jusqu’à ce que la cause soit identifiée.
L’efficacité et l’innocuité de la ciclosporine n’ont pas été évaluées chez les chats âgés de moins de 6 mois et pesant moins de 2,3 kg.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
L’ingestion accidentelle de ce médicament vétérinaire peut entraîner des nausées et / ou des vomissements. Pour éviter toute ingestion accidentelle, le médicament vétérinaire doit être utilisé et gardé hors de portée des enfants. Ne pas laisser la seringue sans surveillance en présence des enfants. Tout aliment pour chat mélangé avec le médicament et non consommé doit être immédiatement retiré et le bol soigneusement lavé. En cas d’ingestion accidentelle, en particulier par un enfant, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette. La ciclosporine peut déclencher des réactions d’hypersensibilité (allergiques). Les personnes présentant une hypersensibilité connue à la ciclosporine doivent éviter tout contact avec le médicament vétérinaire. Ce produit peut causer une irritation en cas de contact avec les yeux. Éviter le contact avec les yeux. En cas de contact, rincer abondamment à l’eau claire. Se laver les mains et la peau exposée après utilisation.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
Aucune.
3.6 Effets indésirables
Concernant les affections malignes, voir les rubriques 3.3 « Contre-indications » et 3.5 « Précautions particulières d’emploi ».
Chiens :
Peu fréquent (1 à 10 animaux / 1 000 animaux traités) : | Troubles gastro-intestinaux (par exemple vomissements, selles molles ou mucoïdes et diarrhées)2,4 Léthargie4, Anorexie4 Hyperactivité4, Hyperplasie gingivale1,4, Réactions cutanées (telles que lésion verruciforme ou modification du pelage)4, Pavillon auriculaire rouge et pavillon auriculaire gonflé4, Faiblesse musculaire ou crampes musculaires4 |
Très rare ( < 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Diabète sucré3 |
Fréquence indéterminée | Hypersalivation2,4 |
1 Légère ou modérée.
2 Légers et transitoires et ne nécessitent généralement pas l’arrêt du traitement.
3 En particulier chez le West Highland White Terrier.
4 Disparaissent généralement spontanément à l’arrêt du traitement.
Chats :
Très fréquent ( > 1 animal / 10 animaux traités) : | Troubles gastro-intestinaux (par exemple vomissements et diarrhée), perte de poids1 |
Fréquent (1 à 10 animaux / 100 animaux traités) : | Augmentation de l’appétit,
Léthargie, Anorexie, Hypersalivation, Hyperactivité, Polydipsie, Hyperplasie gingivale et Lymphadénopathie2 |
1 Généralement légers et transitoires et ne nécessitent pas l’arrêt du traitement.
2 Disparaissent généralement spontanément après l’arrêt du traitement ou après une diminution de la fréquence d’administration.
Les effets secondaires peuvent être graves chez certains animaux.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la rubrique « coordonnées » de la notice.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation :
Chez l’animal de laboratoire, aux doses induisant une materno-toxicité (rats à 30 mg/kg de poids corporel et lapins à 100 mg/kg de poids corporel), la ciclosporine est embryo- et fœtotoxique, par augmentation de la mortalité pré- et postnatale et induit un retard staturo-pondéral du fœtus. Aux doses bien tolérées (rats jusqu’à 17 mg/kg de poids corporel et lapins jusqu’à 30 mg/kg de poids corporel), la ciclosporine n’a pas montré d’effet tératogène ni d’effets sur la reproduction. Par conséquent, l’utilisation n’est pas recommandée chez les chiennes et les chattes gestantes.
Lactation :
Chez l’animal de laboratoire, la ciclosporine passe la barrière placentaire et est excrétée dans le lait. Par conséquent, le traitement des chiennes et des chattes allaitantes n’est pas recommandé.
Fertilité :
L’innocuité du médicament vétérinaire n’a pas été établie chez les chiens ou les chats mâles reproducteurs. En l’absence de telles études, il est recommandé de n’utiliser le médicament vétérinaire chez les animaux reproducteurs qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
3.8 Interactions médicamenteuses et autres formes d'interactions
Diverses substances peuvent inhiber ou stimuler de façon compétitive les enzymes qui interviennent dans le métabolisme de la ciclosporine, en particulier le cytochrome P450 (CYP 3A 4). Dans certains cas cliniquement justifiés, un ajustement de la posologie de la spécialité peut être nécessaire.
Il est connu que la classe des composés des azolés (par exemple : le kétoconazole) augmente les concentrations sanguines de la ciclosporine chez les chiens et les chats, ce qui peut être cliniquement significatif. Il est reconnu que le kétoconazole à la dose de 5 à 10 mg/kg augmente les concentrations sanguines de ciclosporine jusqu’à cinq fois chez le chien et le chat. Lors de l’utilisation concomitante de kétoconazole et de ciclosporine, le vétérinaire doit envisager la possibilité de doubler l’intervalle de traitement si le chien suit un traitement journalier. Les macrolides tels que l’érythromycine peuvent augmenter les concentrations plasmatiques de ciclosporine jusqu’à deux fois. Certains inducteurs du cytochrome P450, anticonvulsivants et antibiotiques (par exemple : triméthoprime/sulfadimidine) peuvent diminuer la concentration plasmatique de la ciclosporine.
La ciclosporine est un substrat et un inhibiteur du transporteur MDR 1 de la glycoprotéine P. Par conséquent, la co-administration de ciclosporine avec des substrats de la glycoprotéine P tels que les lactones macrocycliques (par exemple : ivermectine et milbémycine) peut diminuer l’efflux de ces molécules au niveau des cellules de la barrière hémato-encéphalique, ce qui peut provoquer des signes de toxicité du système nerveux central.
La ciclosporine peut augmenter la néphrotoxicité des antibiotiques de la famille des aminoglycosides et du triméthoprime. L’administration concomitante de la ciclosporine n’est pas recommandée avec ces substances actives.
La vaccination ainsi que l’administration concomitante d’agents immunosuppresseurs doivent faire l’objet d’une attention particulière (voir les rubriques 3.3 « Contre-indications » et 3.5 « Précautions particulières d'emploi »).
3.9 Voies d'administration et posologie
Voie orale.
Avant d’initier le traitement, il faudra déterminer quelles sont les options thérapeutiques alternatives.
Le poids des animaux doit être déterminé avec précision avant l'administration du produit.
Chiens :
La dose moyenne recommandée est de 5 mg de ciclosporine par kg de poids corporel (0,05 mL de solution buvable par kg de poids corporel) et elle doit être administrée quotidiennement en début de traitement. La fréquence de l’administration doit ensuite être réduite en fonction du résultat clinique.
Initialement, le médicament vétérinaire doit être administré une fois par jour jusqu'à obtention d'une amélioration clinique satisfaisante. Celle-ci est généralement observée dans les 4 à 8 semaines. Si aucun effet n'est obtenu dans les 8 premières semaines, le traitement devra être interrompu.
Une fois les signes cliniques de la dermatite atopique correctement contrôlés, le médicament vétérinaire peut alors être administré un jour sur deux en dose d'entretien. Le vétérinaire doit refaire son évaluation clinique à intervalles réguliers et adapter la fréquence d'administration en fonction des résultats cliniques obtenus.
Dans certains cas, quand les signes cliniques sont correctement contrôlés avec un traitement un jour sur deux, le vétérinaire peut décider de prescrire le médicament tous les 3 à 4 jours. La fréquence d’administration efficace la plus basse doit être utilisée afin de maintenir la rémission des symptômes cliniques.
Les patients doivent être réexaminés régulièrement et des traitements alternatifs envisagés. Les traitements d'appoint (par exemple : shampooings médicamenteux, acides gras) peuvent être envisagés avant de réduire l'intervalle de traitement.
Ajuster la durée du traitement en fonction des résultats cliniques. Le traitement peut être arrêté quand les signes cliniques sont contrôlés. En cas de récidive de ces signes, le traitement doit être repris à doses journalières, et dans certains cas des cures répétées peuvent être nécessaires.
Dosage pour chiens :
A la dose standard de 5 mg/kg
Poids (kg) | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | |
Dose (mL) | 0,1 | 0,15 | 0,2 | 0,25 | 0,3 | 0,35 | 0,4 | 0,45 | 0,5 | |
Poids (kg) | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
Dose (mL) | 0,55 | 0,6 | 0,65 | 0,7 | 0,75 | 0,8 | 0,85 | 0,9 | 0,95 | 1 |
Poids (kg) | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
Dose (mL) | 1,05 | 1,1 | 1,15 | 1,2 | 1,25 | 1,3 | 1,35 | 1,4 | 1,45 | 1,5 |
Poids (kg) | 31 | 32 | 33 | 34 | 35 | 36 | 37 | 38 | 39 | 40 |
Dose (mL) | 1,55 | 1,6 | 1,65 | 1,7 | 1,75 | 1,8 | 1,85 | 1,9 | 1,95 | 2 |
Poids (kg) | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 | 49 | 50 |
Dose (mL) | 2,05 | 2,1 | 2,15 | 2,2 | 2,25 | 2,3 | 2,35 | 2,4 | 2,45 | 2,5 |
Poids (kg) | 51 | 52 | 53 | 54 | 55 | 56 | 57 | 58 | 59 | 60 |
Dose (mL) | 2,55 | 2,6 | 2,65 | 2,7 | 2,75 | 2,8 | 2,85 | 2,9 | 2,95 | 3 |
Poids (kg) | 61 | 62 | 63 | 64 | 65 | 66 | 67 | 68 | 69 | 70 |
Dose (mL) | 3,05 | 3,1 | 3,15 | 3,2 | 3,25 | 3,3 | 3,35 | 3,4 | 3,45 | 3,5 |
Poids (kg) | 71 | 72 | 73 | 74 | 75 | 76 | 77 | 78 | 79 | 80 |
Dose (mL) | 3,55 | 3,6 | 3,65 | 3,7 | 3,75 | 3,8 | 3,85 | 3,9 | 3,95 | 4 |
CONDITIONNEMENT PRIMAIRE TYPE 1
Pour les flacons de 30 et 60 mL, une seringue de 1 mL (avec graduations de 0,05 mL) ou une seringue de 2 mL (avec graduations de 0,1 mL) peut être utilisée pour obtenir les doses du tableau ci-dessus, selon le poids de l’animal.
CONDITIONNEMENT PRIMAIRE TYPE 2
Pour les flacons de 30 et 50 mL, une seringue de 1 mL (avec graduations de 0,05 mL) ou une seringue de 3 mL (avec graduations de 0,1 mL) peut être utilisée pour obtenir les doses du tableau ci-dessus, selon le poids de l’animal.
Chats :
La dose moyenne recommandée de ciclosporine est de 7 mg par kg de poids corporel (0,07 mL de solution buvable par kg de poids corporel) et doit être administrée quotidiennement en début de traitement.
La fréquence de l’administration doit ensuite être réduite en fonction du résultat clinique.
Initialement, le médicament vétérinaire doit être administré une fois par jour jusqu'à obtention d'une amélioration clinique satisfaisante (évaluée par l’intensité du prurit et la sévérité des lésions – excoriation, dermatite miliaire, plaques éosinophiliques et/ou alopécie auto-induite). Celle-ci est généralement observée dans les 4 à 8 semaines. Un prurit sévère prolongé peut induire un état d’anxiété et par conséquent un comportement de toilettage excessif. Dans ce cas, malgré une amélioration du prurit lié à l’administration du médicament, la résolution de l’alopécie auto-induite peut être retardée.
Une fois les signes cliniques de la dermatite allergique correctement contrôlés, le médicament vétérinaire peut alors être administré un jour sur deux. Dans certains cas, quand les signes cliniques sont correctement contrôlés avec un traitement un jour sur deux, le vétérinaire peut décider de prescrire le médicament tous les 3 à 4 jours. Il faudra utiliser la fréquence d’administration efficace la plus basse afin de maintenir la rémission des symptômes cliniques.
Les patients doivent être réexaminés régulièrement et des traitements alternatifs envisagés. Ajuster la durée du traitement en fonction des résultats cliniques. Le traitement peut être arrêté quand les signes cliniques sont contrôlés. En cas de récidive de ces signes, le traitement doit être repris à doses journalières, et dans certains cas, des cures répétées peuvent être nécessaires.
Le médicament vétérinaire peut être administré mélangé avec de la nourriture ou directement dans la bouche. Si elle est administrée avec de la nourriture, la solution doit être mélangée avec une petite quantité de nourriture, de préférence après une période de jeûne suffisante pour assurer une consommation complète par le chat. Si le chat n’accepte pas le produit mélangé avec de la nourriture, il doit être administré en insérant la seringue orale directement dans la bouche du chat et en lui administrant toute la dose. Dans le cas où le chat ne consomme que partiellement le produit mélangé avec de la nourriture, l’administration du médicament vétérinaire avec la seringue orale doit être reprise seulement le jour suivant. Tout aliment pour chat mélangé avec le médicament et non consommé doit être immédiatement retiré et le bol soigneusement lavé.
L'efficacité et la tolérance de ce médicament vétérinaire ont été démontrées dans des études cliniques d'une durée de 4,5 mois.
Dosage pour chats :
L’efficacité et l’innocuité de la ciclosporine n’ayant pas été évaluées chez les chats pesant moins de 2,3 kg (voir la rubrique 3.5 « Précautions particulières d'emploi »), l’administration du médicament vétérinaire aux chats pesant moins de 2,3 kg devra se faire après évaluation du rapport bénéfice/risque par le vétérinaire.
Dose standard de 7 mg/kg.
Poids (kg) | 2,1 | 2,9 | 3,6 | 4,3 | 5,0 | 5,7 | 6,4 | 7,1 |
Dosage (mL) | 0,15 | 0,20 | 0,25 | 0,30 | 0,35 | 0,40 | 0,45 | 0,50 |
Poids (kg) | 7,9 | 8,6 | 9,3 | 10,0 | 10,7 | 11,4 | 12,1 | 12,8 | 13,6 | 14,3 |
Dosage (mL) | 0,55 | 0,60 | 0,65 | 0,70 | 0,75 | 0,80 | 0,85 | 0,90 | 0,95 | 1,00 |
CONDITIONNEMENT PRIMAIRE TYPE 1
Pour les flacons de 30 et 60 mL, une seringue de 1 mL (avec graduations de 0,05 mL) ou une seringue de 2 mL (avec graduations de 0,1 mL) peut être utilisée pour obtenir les doses du tableau ci-dessus, selon le poids de l’animal.
CONDITIONNEMENT PRIMAIRE TYPE 2
Pour les flacons de 30 et 50 mL, une seringue de 1 mL (avec graduations de 0,05 mL) ou une seringue de 3 mL (avec graduations de 0,1 mL) peut être utilisée pour obtenir les doses du tableau ci-dessus, selon le poids de l’animal.
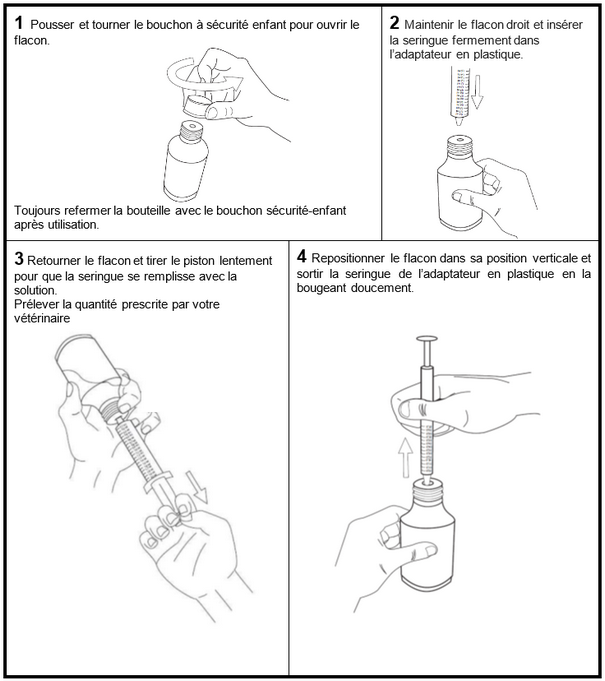
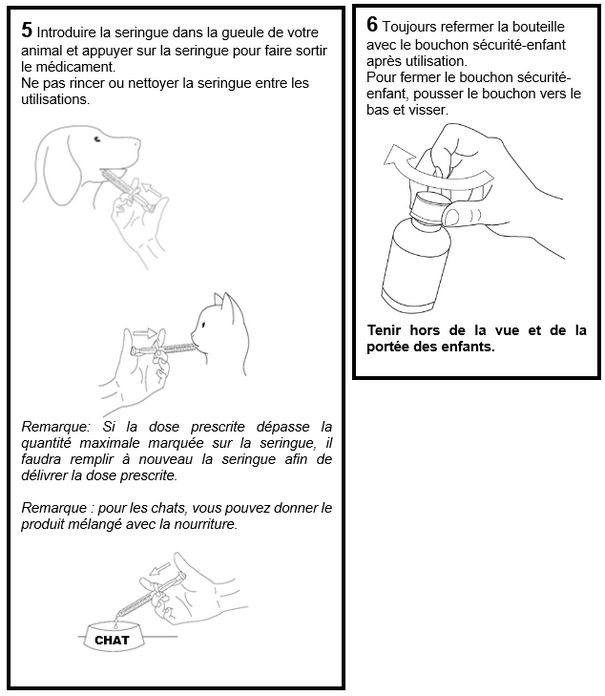
CONSIGNES D’UTILISATION
Chiens : Le médicament vétérinaire doit être donné au moins 2 heures avant ou après le repas. Placer la seringue directement dans la gueule du chien.
Chats : le produit peut être donné mélangé avec la nourriture ou directement dans la gueule du chat.
CONDITIONNEMENT PRIMAIRE TYPE 1
CONDITIONNEMENT PRIMAIRE TYPE 2

Si nécessaire, l’utilisateur peut nettoyer l’extérieur de la seringue avec un chiffon sec et le jeter immédiatement après.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Il n'y a pas d'antidote spécifique et en cas de signes de surdosage, l'animal doit être traité symptomatiquement.
Chiens :
Aucun effet indésirable autre que ceux observés aux doses recommandées n'a été observé chez le chien lors d'administration orale unique d'une dose allant jusqu'à 6 fois la dose recommandée.
De plus, les effets secondaires ci-après ont été observés en cas de surdosage pendant 3 mois ou plus, à quatre fois la dose recommandée : hyperkératose en particulier les pavillons auriculaires, lésion calleuse des coussinets, perte de poids ou diminution de la prise de poids, hypertrichose, augmentation de la vitesse de sédimentation, diminution du taux d'éosinophiles. La fréquence et la sévérité de ces signes sont dose-dépendantes.
Ces signes sont réversibles dans les 2 mois qui suivent l’arrêt du traitement.
Chats :
Les effets indésirables suivants ont été observés en cas d'administration réitérée pendant 56 jours à 24 mg/kg (plus de 3 fois la dose recommandée) ou pendant 6 mois jusqu'à 40 mg/kg (plus de 5 fois la dose recommandée) : fèces liquides / molles, vomissements, augmentations légères à modérées du nombre de neutrophiles, du fibrinogène et du temps de céphaline activé (TCA), légères augmentations de la glycémie et hypertrophie gingivale réversible. Une augmentation de l'appétit a été observée pour les deux schémas posologiques. Une augmentation transitoire suivie d'une diminution du nombre de lymphocytes a été observée chez les chats traités, combinée à une plus grande fréquence de petits nœuds lymphatiques périphériques palpables. Ceci peut refléter une immunosuppression suite à une exposition prolongée à la ciclosporine. Le TCA était augmenté chez les chats ayant reçu au moins deux fois la dose recommandée de ciclosporine. La fréquence et la gravité de ces signes dépendaient généralement de la dose administrée et du temps de traitement. À 3 fois la dose recommandée administrée quotidiennement pendant près de 6 mois, des modifications de l'ECG (troubles de la conduction) se produisent fréquemment. Elles sont transitoires et ne sont pas associées à des signes cliniques. L'anorexie, la position couchée, la perte d'élasticité de la peau, la diminution ou l'absence de fèces, des paupières minces et fermées peuvent être observés dans des cas sporadiques à 5 fois la dose recommandée.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QL04AD01.
4.2 Propriétés pharmacodynamiques
La ciclosporine (aussi appelée cyclosporin, cyclosporine, cyclosporine A, CsA) est un immunosuppresseur sélectif. C'est un polypeptide cyclique à 11 acides aminés d'un poids moléculaire de 1203 daltons qui agit spécifiquement et réversiblement sur les lymphocytes T.
La ciclosporine possède des effets anti-inflammatoires et antiprurigineux dans le traitement de la dermatite atopique et allergique. Il a été démontré qu'elle agit en inhibant principalement l'activation des lymphocytes T lors de stimulation antigénique par inhibition de la synthèse d'IL-2 et d'autres cytokines dérivées de lymphocytes T. La ciclosporine a aussi la capacité d'inhiber la fonction de présentation de l'antigène au niveau du système immunitaire cutané. Elle bloque également le recrutement et l'activation des éosinophiles, la production de cytokines par les kératinocytes, les fonctions des cellules de Langerhans, la dégranulation des mastocytes et donc la libération d'histamine et de cytokines pro-inflammatoires.
La ciclosporine ne déprime pas l'hématopoïèse et ne modifie pas la fonction phagocytaire.
4.3 Propriétés pharmacocinétiques
Chiens :
Absorption
La biodisponibilité de la ciclosporine est d'environ 35 %. Le pic de concentration plasmatique est atteint en 1 à 2 heures. La biodisponibilité est meilleure et moins sujette aux variations individuelles si l'administration a lieu à jeun plutôt qu'au moment du repas.
Distribution
Le volume de distribution est d'environ 7,8 L/kg. La ciclosporine est largement distribuée dans tous les tissus. Suite à l'administration journalière chez le chien, la concentration de ciclosporine est bien plus importante dans la peau que dans le sang.
Métabolisme
La ciclosporine inchangée représente environ 25 % des concentrations sanguines circulantes au cours des 24 premières heures.
La ciclosporine est fortement métabolisée par le cytochrome P450 (CYP 3A 4), principalement au niveau du foie mais aussi de l'intestin. Les réactions sont essentiellement des hydroxylations et des déméthylations qui produisent des métabolites avec peu ou pas d'activité.
Elimination
L'élimination est essentiellement fécale. Seuls 10 % sont éliminés par voie urinaire, surtout sous forme de métabolites.
Aucune accumulation significative dans le sang n'a été observée chez les chiens traités pendant un an.
Chats :
Absorption
La biodisponibilité de la ciclosporine administrée par voie orale est comprise entre 25 et 29 % chez les chats. Les concentrations sanguines maximales sont généralement atteintes en 1 à 2 heure(s) lorsqu'elles sont administrées à des chats à jeun. Les courbes de concentration du médicament dans le sang ne sont pas proportionnelles à la dose à des doses supérieures à la dose recommandée. Il y a une augmentation moins que proportionnelle de la Cmax et de l'ASC pour la plage de dose de 8 à 40 mg/kg.
Distribution
Le volume de distribution à l'état d'équilibre est d'environ 1,7-2,1 L/kg.
Métabolisme
La ciclosporine est métabolisée dans le foie par les enzymes du cytochrome P450 3A.
Élimination
La demi-vie de la phase d'élimination terminale est de 8-11 h.
Il n'y a pas d'accumulation significative de ciclosporine au-delà de la première semaine de traitement.
Chez le chat, il existe de grandes variations inter-individuelles dans les concentrations de ciclosporine dans le sang. À la posologie recommandée, les concentrations plasmatiques de ciclosporine ne sont pas prédictives de la réponse clinique ; par conséquent, la surveillance des taux sanguins n'est pas recommandée.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
En l'absence d'études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé avec d'autres médicaments vétérinaires.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 2 ans.
Durée de conservation après première ouverture du conditionnement primaire : 6 mois.
5.3 Précautions particulières de conservation
Conserver le flacon dans l'emballage extérieur.
Ne pas conserver au réfrigérateur.
Une formation de consistance gélatineuse peut survenir en-dessous de 15°C, ce qui est réversible à des températures supérieures à 25°C, sans conséquence pour la qualité du produit.
Après première ouverture : À conserver à une température ne dépassant pas 25 °C.
5.4 Nature et composition du conditionnement primaire
Conditionnement 1 :
Flacon en verre ambré (type III) fermé par un bouchon à sécurité pour enfant HDPE incluant un adaptateur en plastique (HDPE).
Flacon de 5 mL avec un kit distributeur composé d’une seringue orale PE de 1 mL graduée par incréments de 0,05 mL, conditionnés dans une boîte en carton.
Flacon de 15 mL avec un kit distributeur composé d’une seringue orale PE de 1 mL graduée par incréments de 0,05 mL, conditionnés dans une boîte en carton.
Flacon de 30 mL, avec deux kits distributeurs comprenant une seringue orale PE de 1 mL et une seringue orale PE de 2 mL, graduées respectivement par incréments de 0,05 mL et 0,1 mL, conditionnés dans une boîte en carton.
Flacon de 60 mL, avec deux kits distributeurs comprenant une seringue orale PE de 1 mL et une seringue orale PE de 2 mL, graduées respectivement par incréments de 0,05 mL et 0,1 mL, conditionnés dans une boîte en carton.
Conditionnement 2 :
Flacon en verre ambré (type III) fermé par un bouchon en bromobutyle de 20 mm et un opercule en aluminium rabattable.
Flacon de 5 mL avec un kit distributeur composé d’un capuchon en polycarbonate avec une valve en silicone et d’une seringue orale en polypropylène de 1 mL graduée par incréments de 0,05 mL, conditionnés dans une boîte en carton.
Flacon de 15 mL avec un kit distributeur composé d’un capuchon polycarbonate avec une valve en silicone et d’une seringue orale en polypropylène de 1 mL graduée par incréments de 0,05 mL, conditionnés dans une boîte en carton.
Flacon de 30 mL, avec deux kits distributeurs composés d’un capuchon en polycarbonate avec une valve en silicone et de seringues orales en polypropylène de 1 mL et 3 mL, graduées respectivement par incréments de 0,05 mL et 0,1 mL, emballés dans une boîte en carton.
Flacon de 50 mL, avec deux kits de distributeurs composés d’un capuchon en polycarbonate avec une valve en silicone et de seringues orales en polypropylène de 1 mL et 3 mL, graduées respectivement par incréments de 0,05 mL et 0,1 mL, emballés dans une boîte en carton.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
VIRBAC
1ERE AVENUE 2065 M L I D
06516 CARROS CEDEX
FRANCE
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/2417579 9/2014
Boîte de 1 flacon de 5 mL et de 1 seringue de 1 mL graduée tous les 0,05 mL (conditionnement 1)
Boîte de 1 flacon de 15 mL et de 1 seringue de 1 ml graduée tous les 0,05 mL (conditionnement 1)
Boîte de 1 flacon de 30 mL et de 1 seringue de 1 mL graduée tous les 0,05 mL et de 1 seringue de 2 mL graduée tous les 0,1 mL (conditionnement 1)
Boîte de 1 flacon de 60 mL et de 1 seringue de 1 mL graduée tous les 0,05 mL et de 1 seringue de 2 mL graduée tous les 0,1 mL (conditionnement 1)
Boîte de 1 flacon de 5 mL et de 1 seringue de 1 mL graduée tous les 0,05 mL (conditionnement 2)
Boîte de 1 flacon de 15 mL et de 1 seringue de 1 mL graduée tous les 0,05 mL (conditionnement 2)
Boîte de 1 flacon de 30 mL et de 1 seringue de 1 mL graduée tous les 0,05 mL et de 1 seringue de 3 mL graduée tous les 0,1 mL (conditionnement 2)
Boîte de 1 flacon de 50 mL et de 1 seringue de 1 mL graduée tous les 0,05 mL et de 1 seringue de 3 mL graduée tous les 0,1 mL (conditionnement 2)
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
03/03/2014 - 23/12/2018
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
21/03/2024
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).