DEHINEXXA 60 MG/15 MG SOLUTION POUR SPOT-ON POUR CHATS MOYENS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque mL contient 85,8 mg de praziquantel et 21,4 mg d'émodepside.
Chaque pipette (0,70 mL) contient : |
|
|
|
Substances actives : |
|
Praziquantel | 60 mg |
Emodepside | 15 mg |
Excipients :
Composition qualitative en excipients et autres composants | Composition quantitative si cette information est essentielle à une bonne administration du médicament vétérinaire |
Butylhydroxyanisole (E320) | 3,78 mg |
Isopropylidène glycérol |
|
Acide lactique |
|
Solution limpide, incolore à jaune ou brune.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chats (> 2,5 - 5 kg).
3.2 Indications d'utilisation pour chaque espèce cible
Pour les chats atteints, ou à risque, d'infections parasitaires mixtes causées par les vers ronds et les vers plats et des vers pulmonaires, ciblés par chacun des principes actifs combinés. Le médicament vétérinaire n'est indiqué que lorsqu'une utilisation simultanée contre les vers ronds et les vers plats est nécessaire.
Vers ronds (Nématodes) :
Toxocara cati (stade adulte mature, stade adulte immature et stades larvaires L3 et L4).
Toxocara cati (stade larvaire L3) – traitement des femelles en fin de gestation en prévention d’une transmission à la portée via l’allaitement.
Toxascaris leonina (stade adulte mature, stade adulte immature et stade larvaire L4).
Ancylostoma tubaeforme (stade adulte mature, stade adulte immature et stade larvaire L4).
Vers plats (Cestodes) :
Dipylidium caninum (stade adulte mature et stade adulte immature).
Taenia taeniaeformis (stade adulte).
Echinococcus multilocularis (stade adulte).
3.3 Contre-indications
Ne pas utiliser chez les chatons ou les chats pesant moins de 2,5 kg.
Ne pas utiliser en cas d’hypersensibilité aux substances actives ou à l’un des excipients.
3.4 Mises en garde particulières
L'utilisation inutile d'antiparasitaires ou une utilisation non conforme aux instructions du RCP peut accroître la pression de sélection de la résistance et entraîner une diminution de l'efficacité. La décision d'utiliser le produit doit être basée sur la confirmation de l'espèce parasitaire et de la charge parasitaire, ou du risque lié à ses caractéristiques épidémiologiques, pour chaque animal.
En l'absence de risque de co-infection, un produit à spectre étroit doit être utilisé.
La possibilité que d'autres animaux du même foyer soient une source de réinfection par des nématodes et/ou des cestodes doit être envisagée, et ces animaux doivent être traités si nécessaire avec un produit approprié.
Lorsqu'une infection par le cestode Dipylidium caninum est confirmée, un traitement concomitant contre les hôtes intermédiaires, tels que les puces et les poux, doit être discuté avec un vétérinaire afin de prévenir une réinfection.
La résistance d’un parasite à une classe particulière d’anthelminthiques, quelle qu’elle soit, peut se développer suite à l’usage fréquent et répété d’un anthelminthique de cette classe.
Une résistance de Dipylidium caninum au praziquantel a été signalée chez le chien.
L'utilisation de ce produit doit tenir compte des informations locales sur la sensibilité des parasites cibles, lorsqu'elles sont disponibles.
Il est recommandé d'enquêter plus en détail sur les cas de résistance suspectée, en utilisant une méthode de diagnostic appropriée.
Toute résistance confirmée doit être signalée au titulaire de l'autorisation de mise sur le marché ou aux autorités compétentes.
Un shampoing ou une immersion de l’animal dans l’eau directement après le traitement peut réduire l’efficacité du médicament vétérinaire. C’est pourquoi les animaux traités ne doivent pas être baignés jusqu’à ce que la solution ait complètement séché.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Appliquer seulement sur la surface de la peau et sur une peau intacte. Ne pas faire avaler et ne pas administrer par voie parentérale.
Éviter que le chat traité ou les autres chats de la famille lèchent le site d’application du médicament vétérinaire tant qu’il est humide.
L'expérience est limitée concernant l'utilisation du médicament vétérinaire sur les animaux malades ou affaiblis, par conséquent, le médicament vétérinaire ne doit être utilisé que sur la base d'une évaluation du rapport bénéfice-risque pour ces animaux.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Ce médicament vétérinaire peut être irritant pour la peau et les yeux.
En cas de contact accidentel avec la peau, lavez immédiatement la peau à l’eau et au savon.
Si le médicament vétérinaire entre accidentellement en contact avec les yeux, ceux-ci doivent être soigneusement rincés à grande eau.
Si les symptômes cutanés ou oculaires persistent, ou en cas d'ingestion accidentelle, consultez immédiatement un médecin et montrez-lui la notice ou l'étiquette.
Éviter tout contact direct avec la zone d'application lorsqu'elle est humide. Veiller à ce que les enfants n'aient pas de contact intensif prolongé (par exemple, en dormant) avec les chats traités pendant les 24 heures suivant l'application du médicament vétérinaire.
Ne pas fumer, manger ni boire pendant l'application.
Se laver les mains après utilisation.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
Le solvant contenu dans ce médicament vétérinaire pourrait tacher certains matériaux tels que le cuir, les tissus, plastiques et surfaces vernies. S’assurer que le site d’application est sec avant de permettre tout contact avec de tels matériaux.
L’échinococcose représente un danger pour l’Homme. L’échinococcose est une maladie à déclaration obligatoire auprès de l’OMSA, les instructions spécifiques de traitement, de suivi et de protection des personnes sont à demander aux autorités compétentes concernées.
3.6 Effets indésirables
Chats :
Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Alopécie au site d'application1, prurit au site d'application1, inflammation au site d'application1 Salivation2, vomissements2, diarrhée2, anorexie Troubles neurologiques (légers et transitoires)2, 3 Troubles comportementaux4 |
1 Transitoire.
2 Ces symptômes résulteraient du léchage du site d'application par le chat, immédiatement après le traitement.
3 Comme de l’ataxie ou des tremblements.
4 Comme de l'hyperactivité, l'anxiété et la vocalisation.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation et lactation :
Peut être utilisé au cours de la gestation et la lactation.
3.8 Interactions médicamenteuses et autres formes d'interactions
L’émodepside est un substrat pour la glycoprotéine P. Des traitements simultanés avec d’autres médicaments qui sont des substrats/inhibiteurs de la glycoprotéine P (par exemple, l’ivermectine et d’autres lactones macrocycliques antiparasitaires, l’érythromycine, la prednisolone ou la ciclosporine) pourraient conduire à des interactions médicamenteuses pharmacocinétiques. Les conséquences cliniques potentielles de telles interactions n’ont pas été évaluées. Si votre chat reçoit des médicaments, veuillez prendre contact avec votre vétérinaire pour en discuter avant d'appliquer le médicament vétérinaire. De même, veuillez informer votre vétérinaire que vous utilisez ce médicament vétérinaire s'il administre un médicament à votre chat.
3.9 Voies d'administration et posologie
Administration par spot-on.
Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible. Un sous-dosage pourrait entraîner une utilisation inefficace et favoriser le développement d’une résistance.
Posologie et calendrier du traitement
Les doses minimales recommandées sont de 12 mg de praziquantel/kg de poids corporel et 3 mg d’émodepside/kg de poids corporel, équivalant à 0,14 mL de médicament vétérinaire/kg de poids corporel.
Poids corporel du chat (kg) | Taille/volume de la pipette (mL) à utiliser | Praziquantel (mg/kg de poids corporel) | Émodepside (mg/kg de poids corporel) |
> 2,5 - 5 | 0,70 | 12 - 24 | 3 - 6 |
Pour le traitement des vers ronds et des vers plats, une seule administration est efficace.
Pour le traitement des femelles gestantes en prévention de la contamination avec Toxocara cati (stade larvaire L3) via l’allaitement aux chatons, une administration unique approximativement sept jours avant la date estimée de mise-bas est efficace.
Mode d’administration
Pour application externe uniquement.
1. Sortir une pipette de son emballage. Tenir la pipette en position verticale, tourner et retirer le capuchon.
2. Retournez le bouchon et replacez l'autre extrémité sur la pipette. Poussez et tournez le bouchon pour rompre l'opercule, puis retirez-le de la pipette.
3. Écarter les poils sur la nuque de l'animal, à la base du crâne, de façon à voir la peau. Placez l’extrémité de la pipette sur la peau et presser fermement plusieurs fois pour vider complètement son contenu directement sur la peau en un endroit. Évitez tout contact entre le médicament vétérinaire et vos doigts.
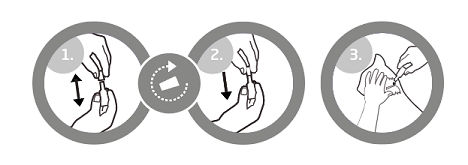
L’application à la base du crâne permettra de minimiser les possibilités de léchage du médicament vétérinaire par l’animal.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Une salivation, des vomissements et des signes neurologiques (tremblements) ont été observés de façon occasionnelle après application de doses du médicament vétérinaire allant jusqu’à 10 fois la dose recommandée chez les chats adultes et jusqu’à 5 fois la dose recommandée chez les chatons. Ces symptômes résulteraient du léchage du site d'application par le chat. Les symptômes étaient totalement réversibles.
Il n’y a pas d’antidote spécifique connu.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QP52AA51
4.2 Propriétés pharmacodynamiques
Le praziquantel est un dérivé de la pyrazinoisoquinoléine et est efficace contre les vers plats comme Dipylidium caninum, Echinococcus multilocularis et Taenia taeniaeformis.
Le praziquantel est rapidement absorbé par la surface du parasite et agit essentiellement en modifiant la perméabilité au Ca++ des membranes du parasite. Cela entraîne des dommages sévères du tégument du parasite, des contractions, une paralysie et une perturbation du métabolisme, entraînant finalement la mort du parasite.
L’émodepside est un composé semi-synthétique appartenant à la nouvelle classe chimique des depsipeptides. Il est actif contre les vers ronds (ascaris et ankylostomes). Dans ce médicament vétérinaire, l’émodepside est responsable de l’efficacité contre Toxocara cati, Toxascaris leonina, Ancylostoma tubaeforme et Aelurostrongylus abstrusus.
Il agit au niveau des jonctions neuromusculaires en stimulant les récepteurs présynaptiques qui font partie de la famille des récepteurs de sécrétine, ce qui entraîne la paralysie et la mort des parasites.
4.3 Propriétés pharmacocinétiques
Après application cutanée de ce médicament vétérinaire chez les chats à la dose minimale thérapeutique de 0,14 mL/kg de poids corporel, on observe des concentrations maximales sériques moyennes de 32,2 ± 23,9 μg/L d’émodepside et 61,3 ± 44,1 μg/L de praziquantel. Ces concentrations maximales sont atteintes 18,7 ± 47 heures après application pour le praziquantel et 3,2 ± 2,7 jours pour l’émodepside. Les deux principes actifs sont ensuite lentement éliminés du sérum avec une demi-vie de 4,1 ± 1,5 jours pour le praziquantel et 9,2 ± 3,9 jours pour l’émodepside.
Des études réalisées sur plusieurs espèces différentes montrent que le praziquantel est rapidement métabolisé dans le foie. Les principaux métabolites sont les dérivés monohydroxycyclohexyl du praziquantel. L’élimination rénale prédomine. L'excrétion fécale prédomine avec l’émodepside inchangé et des dérivés hydroxylés en principaux produits d'excrétion.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Aucune connue.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 2 ans.
5.3 Précautions particulières de conservation
À conserver dans l’emballage d’origine de façon à le protéger de la lumière et de l’humidité.
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation en ce qui concerne la température.
5.4 Nature et composition du conditionnement primaire
Pipette unidose en polypropylène blanc avec un bouchon en polyéthylène haute densité avec un perforateur, conditionnée dans un sachet en aluminium laminée.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Le médicament vétérinaire ne doit pas être déversé dans les cours d’eau car l’émodepside pourrait mettre les poissons et autres organismes aquatiques en danger.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
KRKA TOVARNA ZDRAVIL D.D. NOVO MESTO
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/8311030 0/2025
Boîte en carton de 1 pipette de 0,70 mL
Boîte en carton de 2 pipettes de 0,70 mL
Boîte en carton de 3 pipettes de 0,70 mL
Boîte en carton de 6 pipettes de 0,70 mL
Boîte en carton de 40 pipettes de 0,70 mL
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
08/07/2025
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
08/07/2025
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).