DERMATT BIOCANINA 0,375 MG / 1,055 MG COMPRIMES PELLICULES POUR CHIENS ET CHATS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un comprimé contient : |
|
|
|
Substances actives : |
|
Dexaméthasone……………………………………………. | 0,375 mg |
Chlorphénamine …………………………………………... | 1,055 mg |
(sous forme de maléate) |
|
(équivalant à 1,50 mg de maléate de chlorphénamine) |
|
|
|
Excipients : |
|
Composition qualitative en excipients et autres composants |
Noyau |
Amidon de maïs prégélatinisé |
Cellulose microcristalline |
Silice colloïdale anhydre |
Stéarate de magnésium |
Pelliculage |
Acétate phtalate de cellulose |
Phtalate de diéthyle |
Comprimés pelliculés de couleur blanche, de forme cylindrique.
Comprimé avec une barre de sécabilité permettant une division en deux fractions égales.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens et chats.
3.2 Indications d'utilisation pour chaque espèce cible
Traitement des états inflammatoires et allergiques.
3.3 Contre-indications
Ne pas utiliser chez les animaux souffrant de diabète sucré, d'hyperadrénocorticisme, d'insuffisance rénale et d'insuffisance cardiaque ou souffrant d'ulcères gastroduodénaux.
Ne pas utiliser chez les animaux atteints de maladie infectieuse, à moins qu'une thérapie anti-infectieuse appropriée soit administrée au même moment.
3.4 Mises en garde particulières
Aucune.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
En cas d'échec ou de rechute rapide, ne pas augmenter les doses et consulter un vétérinaire.
Pendant le traitement, ne pas augmenter les rations habituelles. Il est conseillé, lors de cures prolongées, de diminuer la quantité de sel et de féculents.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
En cas d'ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Les personnes présentant une hypersensibilité connue à la dexaméthasone ou à la chlorphénamine doivent éviter tout contact avec le médicament vétérinaire.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens et chats :
Fréquence indéterminée | Hypercorticisme (iatrogène)1 Polyurie1 Polydipsie1, polyphagie1 Immunodépression1 Redistribution des réserves lipidiques de l’organisme1 |
1signes pouvant être provoqués en cas d'usage prolongé de corticostéroïdes tels que la dexaméthasone.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir également la rubrique « coordonnées » de la notice.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation :
Ne pas utiliser durant la gestation.
3.8 Interactions médicamenteuses et autres formes d'interactions
L'administration concomitante de médicaments anti-inflammatoires non stéroïdiens peut augmenter le risque d'ulcération du tractus gastro-intestinal.
3.9 Voies d'administration et posologie
Voie d'administration : orale.
| Espèce cible | Nombre de comprimés par jour. |
| Chiens nains et chats | 1/2 comprimé 2 fois par jour pendant 5 jours. |
| Petits chiens | 1 comprimé 2 fois par jour pendant 2 jours, puis 1 par jour pendant 3 jours. |
| Chiens moyens | 1 comprimé 3 fois par jour pendant 2 jours, puis 1 comprimé matin et soir pendant 3 jours. |
| Gros chiens | 2 comprimés 2 fois par jour pendant 2 jours, puis 3 par jour pendant 3 jours. |
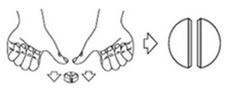
Pour diviser le comprimé en deux parties égales, le placer sur une surface plane avec la face portant la barre de sécabilité tournée vers le haut. Appuyer avec les pouces des deux côtés du comprimé jusqu’à le fractionner.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Aucun.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QH02BX90
4.2 Propriétés pharmacodynamiques
La dexaméthasone est un puissant glucocorticoïde de synthèse possédant une faible activité minéralocorticoïde. La dexaméthasone possède dix à vingt fois l'activité anti-inflammatoire de la prednisolone à dose molaire équivalente. Les corticostéroïdes peuvent diminuer la réponse immunitaire. En effet, ils inhibent la dilatation des capillaires, la migration des leucocytes et la phagocytose. Les glucocorticoïdes ont un effet sur le métabolisme en accroissant la néoglucogenèse. La chlorphénamine est un anti-histaminique de type anti-H1.
4.3 Propriétés pharmacocinétiques
Non documentées.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Non connues.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
5.3 Précautions particulières de conservation
À conserver à une température ne dépassant pas 25º C.
5.4 Nature et composition du conditionnement primaire
Plaquette thermoformée PVC-aluminium-OPA/aluminium
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
DOMES PHARMA
3 RUE ANDRE CITROEN
63430 PONT DU CHATEAU
FRANCE
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/2986723 9/1988
Boîte en carton de 2 plaquettes thermoformées de 10 comprimés pelliculés sécables
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
30/09/1988 - 25/06/2009
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
11/06/2024
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).