FIPROCARE MULTI 134 MG/40 MG SOLUTION POUR SPOT-ON POUR CHIENS MOYENS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque pipette de 1,34 mL contient : |
|
|
|
Substances actives : |
|
Fipronil………………………………………………………. | 134,0 mg |
Pyriproxifène……………………………………………….. | 40,2 mg |
|
|
Excipients : |
|
Composition qualitative en excipients et autres composants | Composition quantitative si cette information est essentielle à une bonne administration du médicament vétérinaire |
Butylhydroxyanisole (E320) | 0,268 mg |
Butylhydroxytoluène (E321) | 0,134 mg |
Éther monoéthylique de diéthylèneglycol |
|
Solution limpide, incolore à jaune pâle.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens (10-20 kg).
3.2 Indications d'utilisation pour chaque espèce cible
A utiliser contre les infestations par les puces seules ou contre celles par les puces et par les tiques.
Contre les puces :
Traitement et prévention des infestations par les puces (Ctenocephalides felis). Une application prévient de toute nouvelle infestation pendant 7 semaines.
Prévention de la multiplication des puces en empêchant le développement des œufs de puce en puces adultes pendant 12 semaines après application.
Contre les tiques :
Traitement des infestations par les tiques (Ixodes ricinus).
Une application permet une efficacité acaricide qui persiste pendant 2 semaines contre Ixodes ricinus et pendant 4 semaines contre Dermacentor reticulatus et Rhipicephalus sanguineus.
Si certaines espèces de tiques (Dermacentor reticulatus, Rhipicephalus sanguineus) sont présentes au moment de l’application, elles peuvent ne pas être toutes tuées dans les 48 heures.
3.3 Contre-indications
Ne pas utiliser chez le lapin, des effets indésirables parfois létaux pouvant survenir.
Ne pas utiliser en cas d'hypersensibilité aux substances actives ou à l'un des excipients.
3.4 Mises en garde particulières
Une baignade ou un shampooing immédiatement après le traitement peuvent réduire la durée d’activité. Le médicament vétérinaire reste efficace contre les puces pendant 5 semaines si le chien est shampouiné tous les mois une fois traité. Si un shampooing s’avère nécessaire, il est recommandé de le faire avant application.
Une baignade à deux reprises après le traitement n’affecte pas l'efficacité adulticide contre les puces, ni l'efficacité de la prévention du développement des œufs de puce en puces adultes.
L'effet de la baignade ou du shampooing du chien sur l'efficacité du médicament vétérinaire contre les tiques n'a pas été évalué.
Dès le début des mesures de contrôle antiparasitaire, en cas d'infestation, le panier de l'animal et ses zones de couchage ou de repos (tapis, canapés …) doivent être traités avec un insecticide approprié et aspirés régulièrement.
Pour réduire la pression parasitaire environnementale liée aux puces, il est recommandé de traiter tous les animaux du foyer avec un produit contre les puces approprié.
Le médicament vétérinaire n'empêche pas les tiques de se fixer aux animaux. La transmission d'une maladie infectieuse par des tiques ne peut donc être complètement exclue en cas de conditions défavorables. Une efficacité immédiate a été démontrée contre Ixodes ricinus, ce qui signifie que les tiques de cette espèce sont généralement tuées dans les 48 heures après l'application du médicament vétérinaire. Si des tiques du type Dermacentor reticulatus ou Rhipicephalus sanguineus sont présentes au moment de l’application, il se peut qu'elles ne soient pas tuées dans les 48 heures.
Une fois mortes, les tiques se détachent souvent de l'animal. Toute tique restante devra être retirée précautionneusement, en s’assurant que les pièces buccales ne restent pas dans la peau.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
À usage externe exclusivement.
Les animaux doivent être pesés avec précision avant le traitement.
En l'absence de données d'innocuité, le médicament vétérinaire ne doit pas être utilisé chez les chiens de moins de 10 semaines et/ou pesant moins de 2 kg.
Éviter tout contact du contenu de la pipette avec les yeux ou la bouche de l’animal. Veiller en particulier à éviter le léchage de la zone d'application du médicament vétérinaire par le chien traité ou par tout autre animal en contact avec lui.
Ne pas appliquer le médicament vétérinaire sur une plaie ou sur une lésion cutanée.
En l'absence d'étude d'innocuité complémentaire, l’intervalle minimum entre deux traitements doit être de 4 semaines.
L'innocuité de ce médicament vétérinaire n'a pas été étudiée chez les chiens malades ou affaiblis.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le médicament vétérinaire peut occasionner des troubles nerveux.
Le médicament vétérinaire peut être nocif en cas d’ingestion.
Éviter d’ingérer le médicament vétérinaire ou de porter la main à la bouche après utilisation.
Ne pas fumer, boire ou manger pendant l’application.
En cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Le médicament vétérinaire peut provoquer une irritation des yeux et des muqueuses.
Éviter tout contact avec la peau, les yeux et la bouche, ce qui inclut le contact main-œil.
En cas de contact cutané ou oculaire accidentel, laver immédiatement et abondamment avec de l’eau. En cas de persistance d’une irritation de la peau ou des yeux, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Se laver les mains après utilisation.
Tant que le site d’application n’est pas sec, ne pas toucher les animaux traités et ne pas laisser les enfants jouer avec eux. Il est donc recommandé de ne pas traiter les animaux pendant la journée mais plutôt en début de soirée, et les animaux une fois traités ne doivent pas être autorisés à dormir avec leurs maîtres, en particulier les enfants.
Conserver les pipettes dans leur emballage d’origine et les éliminer immédiatement après utilisation de façon appropriée.
Précautions particulières concernant la protection de l'environnement
Le fipronil et le pyriproxifène peuvent avoir des effets indésirables sur les organismes aquatiques. Ne pas laisser les chiens se baigner dans les cours d’eau pendant les 48 heures suivant le traitement (voir aussi la rubrique 5.5).
Autres précautions
Le médicament vétérinaire peut avoir des effets indésirables sur les surfaces, matériaux et meubles de la maison. Attendre que le site d’application soit sec avant de permettre le contact avec ces matériaux.
3.6 Effets indésirables
Chiens (10-20 kg) :
Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Réaction au site d’application1 (par exemple, squamosis au site d’application, alopécie au site d’application, prurit au site d’application, érythème au site d’application, altération de la couleur de la peau sur le site d’application)
Prurit généralisé, alopécie
Hypersalivation, vomissements
Troubles neurologiques2 (par exemple, hyperesthésie, dépression du système nerveux central, symptômes neurologiques)
Troubles respiratoires |
Fréquence indéterminée (Ne peut être estimée sur la base des données disponibles) | Poil gras au site d’application1,3, desquamation au site d’application1,3,4 |
1 Transitoires.
2 Réversibles.
3 Effet cosmétique.
4 Légers.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation et de lactation.
Gestation et lactation :
Les études de laboratoire réalisées sur le fipronil et le pyriproxifène n’ont pas mis en évidence d’effets tératogènes ou embryotoxiques. L'utilisationne doit se faire qu'après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
3.8 Interactions médicamenteuses et autres formes d'interactions
Aucune connue.
3.9 Voies d'administration et posologie
Administration par spot-on.
Posologie :
Pour un chien pesant de 10 à 20 kg, appliquer une pipette de 1,34 mL, correspondant à la dose minimale recommandée de 6,7 mg de fipronil par kg de poids corporel et de 2 mg de pyriproxifène par kg de poids corporel.
Poids du chien | Volume de la pipette | Fipronil (mg) | Pyriproxifène (mg) |
2-10 kg | 0,67 mL | 67 | 20,1 |
10-20 kg | 1,34 mL | 134 | 40,2 |
20-40 kg | 2,68 mL | 268 | 80,4 |
40-60 kg | 4,02 mL | 402 | 120,6 |
Pour les chiens de plus de 60 kg, utiliser la combinaison de pipettes appropriée.
Mode d’administration :
Extraire la pipette de sa plaquette. La tenir en position verticale. Tapoter la partie étroite de la pipette pour s'assurer que le contenu est bien descendu dans la partie centrale de la pipette. Rompre l'extrémité autocassable de la pipette en suivant la ligne gravée.
Écarter les poils de l'animal à la base du cou, en avant des omoplates, jusqu’à ce que la peau soit visible. Placer l'embout de la pipette directement sur la peau ainsi exposée. Presser doucement la partie centrale de la pipette plusieurs fois pour en expulser entièrement le contenu. Si nécessaire, en particulier chez les grands chiens, le contenu de la pipette peut être réparti à un ou à deux endroits supplémentaires le long du dos de l'animal pour éviter que le liquide coule sur les flancs ou reste trop superficiellement dans le poil.
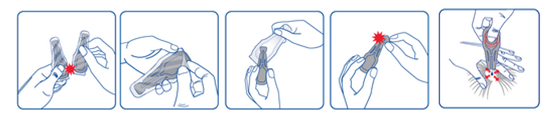
Système anti-goutte (le médicament vétérinaire est libéré uniquement par pression sur la partie centrale de la pipette).

Une pipette correspond à un traitement, qui peut être répété sur la base d’une application par mois.
Pour un contrôle optimal des infestations par les puces et les tiques et de la multiplication des puces, la fréquence d'application peut se baser sur les conditions épidémiologiques locales.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Aucun effet indésirable grave n'a été observé au cours d'une étude d’innocuité réalisée sur des chiots de 10 semaines, traités avec jusqu’à 5 fois la dose maximale recommandée 3 fois à 4 semaines d'intervalle, et traités à la dose maximale recommandée 6 fois à 4 semaines d'intervalle.
Le risque d’effets indésirables (voir rubrique « 3.6 - Effets indésirables ») peut cependant augmenter avec le surdosage, il faut donc toujours traiter les animaux avec la taille de pipette adaptée à leur poids.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QP53AX65.
4.2 Propriétés pharmacodynamiques
Le fipronil est un insecticide et un acaricide de la famille des phénylpyrazolés. Le fipronil et son métabolite, le fipronil sulfone, agissent sur les canaux chlorure activés par des ligands, en particulier les canaux activés par le neurotransmetteur acide gamma-aminobutyrique (GABA) mais aussi les canaux désensibilisants (D) et non-désensibilisants (N) activés par le glutamate (Glu, canaux chlorure ligand-dépendants propres aux Invertébrés). Ils bloquent ainsi le passage pré- et post-synaptique des ions chlorure à travers la membrane cellulaire. Il en résulte une activité incontrôlée du système nerveux central et la mort des insectes ou des acariens.
Le pyriproxifène est un régulateur de la croissance des insectes (RCI) de la classe des analogues de l'hormone juvénile. Le pyriproxifène stérilise les puces adultes et inhibe le développement des stades immatures. La molécule empêche, par contact, l'émergence d'insectes adultes, en bloquant le développement des œufs (effet ovicide), des larves et des pupes (effet larvicide), qui sont ainsi éliminés. Elle agit également par contact et/ou ingestion par les puces adultes en stérilisant les œufs pendant leur maturation et avant la ponte. Enfin, la molécule empêche la contamination de l'environnement des animaux traités par les stades immatures des puces.
L'association du fipronil et du pyriproxifène permet une activité insecticide et acaricide contre les puces (Ctenocephalides felis) et les tiques (Rhipicephalus sanguineus, Dermacentor reticulatus, Ixodes ricinus), et empêche le développement des œufs de puce en puces adultes.
4.3 Propriétés pharmacocinétiques
Dans les conditions normales d’utilisation du médicament vétérinaire, le fipronil et le pyriproxifène sont correctement distribués dans le pelage de l'animal dans les 24 heures suivant l’application topique.
Le métabolite principal du fipronil est son dérivé sulfoné, qui possède également des propriétés insecticides et acaricides.
Les concentrations de fipronil, de fipronil sulfone et de pyriproxifène dans le pelage diminuent progressivement mais sont toujours détectables au moins 84 jours après application.
Le pic de concentration plasmatique du fipronil est atteint entre 3 et 7 jours, et celui du fipronil sulfone entre 7 et 14 jours après administration du médicament vétérinaire. Le pic de concentration plasmatique du pyriproxifène est atteint entre 1 et 3 jours après administration du médicament vétérinaire. Les concentrations plasmatiques du fipronil et du pyriproxifène diminuent progressivement et restent quantifiables jusqu’à 50 jours après application.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Aucune connue.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
5.3 Précautions particulières de conservation
A conserver à une température ne dépassant pas 30°C.
A conserver dans un endroit sec.
Conserver le conditionnement primaire dans leur emballage extérieur de façon àle protéger de la lumière.
5.4 Nature et composition du conditionnement primaire
Pipette unidose plastique transparente thermoformée (polyacrylonitrile méthacrylate ou polyéthylène - éthylène-alcool vinylique – polyéthylène - polypropylène - copolymère d'oléfines cycliques - polypropylène) et thermoscellée par film polyacrylonitrile méthacrylate ou polyéthylène - éthylène-alcool vinylique – polyéthylène - aluminium - polyéthylène téréphtalate
Pipette placée dans plaquette thermoformée (polypropylène - copolymère d'oléfines cycliques - polypropylène) et thermoscellée par film polyéthylène téréphtalate - aluminium - polypropylène
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Le médicament vétérinaire ne doit pas être déversé dans les cours d’eau car le fipronil et le pyriproxifène pourraient mettre les poissons et autres organismes aquatiques en danger.
Ne pas contaminer les étangs, les cours d’eau ou les fossés avec le médicament vétérinaire ou les emballages vides.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
ALFAMED
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/3143886 3/2017
Boîte de 1 pipette de 1,34 mL
Boîte de 2 pipettes de 1,34 mL
Boîte de 3 pipettes de 1,34 mL
Boîte de 4 pipettes de 1,34 mL
Boîte de 6 pipettes de 1,34 mL
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
26/01/2018
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
22/12/2025
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire non soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).