PERGOSAFE 0,25 MG COMPRIMES PELLICULES POUR CHEVAUX
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé contient : | |
Substance(s) active(s): | |
Pergolide…………………………………………………… | 0,25 mg |
(équivalant à 0,33 mg de mésilate de pergolide) |
|
Excipient(s)
Composition qualitative en excipients et autres composants | Composition quantitative si cette information est essentielle à une bonne administration du médicament vétérinaire |
Noyau: | / |
Lactose monohydraté | / |
Croscarmellose sodique | / |
Povidone K30 | / |
Stéarate de magnésium | / |
Oxyde de fer jaune (E172) | 0,03 mg |
Pelliculage : | / |
Poly(alcool vinylique) | / |
Talc | / |
Dioxyde de titane (E171) | 0,708 mg |
Oxyde de fer noir (E172) | 0,042 mg |
Monocaprylocaprate de glycérol | / |
Laurilsulfate de sodium | / |
Comprimé pelliculé de forme sphérique, de couleur grise
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chevaux (non producteur de denrées).
3.2 Indications d'utilisation pour chaque espèce cible
Traitement symptomatique des signes cliniques associés au dysfonctionnement du lobe intermédiaire de l’hypophyse (Pituitary Pars Intermedia Dysfunction, PPID) (maladie de Cushing chez le cheval).
3.3 Contre-indications
Ne pas utiliser chez les chevaux présentant une hypersensibilité connue au mésilate de pergolide ou à d’autres dérivés de l’ergot de seigle ou à l’un des excipients.
Ne pas utiliser chez les chevaux de moins de 2 ans.
3.4 Mises en garde particulières
Des tests diagnostiques endocriniens de laboratoire appropriés doivent être réalisés, ainsi qu’une évaluation des signes cliniques, de façon à établir un diagnostic de PPID.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Comme la majorité des cas de PPID sont diagnostiqués chez des chevaux âgés, d’autres processus pathologiques sont fréquemment présents. Pour la surveillance et la fréquence des tests, voir la rubrique 3.9.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le pergolide, comme les autres dérivés de l’ergot de seigle, peut causer des vomissements, des vertiges, une léthargie ou une baisse de la tension artérielle.
Des effets indésirables sévères, tels que des collapsus, ont été observés. L’ingestion peut être nocive et associée à des effets indésirables sévères, notamment chez les enfants ou les personnes souffrant de troubles cardiaques préexistants. Veiller à prendre toutes les précautions nécessaires pour éviter toute ingestion accidentelle du médicament vétérinaire.
Afin de réduire le risque d’ingestion accidentelle :
- Éviter tout contact main-bouche. Ne pas manger, boire ou fumer lors de la manipulation de ce produit.
- Conserver et manipuler ce médicament vétérinaire séparément des médicaments à usage humain et le manipuler avec une extrême précaution. Replacer la plaquette dans l’emballage et la tenir hors de portée des enfants.
- Les comprimés préparés en vue de l’administration doivent être administrés immédiatement et ne pas être laissés sans surveillance.
En cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette. Évitez de conduire ou d’utiliser des machines en cas d’ingestion de ce médicament vétérinaire.
Ce médicament vétérinaire peut causer une irritation oculaire. Éviter tout contact avec les yeux, y compris les contacts main-yeux, lors de la manipulation des comprimés. Réduire au minimum le risque d’exposition lors de la dissolution des comprimés; p. ex., ne pas broyer les comprimés. En cas de contact du produit dissous avec la peau, laver à l’eau la partie exposée. En cas d’exposition oculaire, rincer immédiatement l’œil atteint avec une grande quantité d’eau et demander conseil à un médecin.
Lavez-vous les mains après utilisation.
Ce médicament vétérinaire peut provoquer des réactions d’hypersensibilité (allergie). Les personnes présentant une hypersensibilité connue au pergolide ou à d’autres dérivés de l’ergot de seigle devraient éviter tout contact avec le médicament vétérinaire.
Ce médicament vétérinaire peut provoquer des effets indésirables dus à la diminution des taux de prolactine, ce qui expose les femmes enceintes et qui allaitent à un risque particulier. Les femmes enceintes ou qui allaitent doivent éviter tout contact dermique ou tout contact main-bouche et doivent porter des gants lors de l’administration du médicament.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chevaux:
Rare (1 à 10 animaux / 10 000 animaux traités) : | Perte d’appétit, anorexie1, léthargie1. Des signes affectant le système nerveux central2 (par exemple, dépression2, ataxie2). Diarrhée, coliques. |
Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Sudation. |
1 transitoires
2 légers
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
L’innocuité de ce médicament vétérinaire n’a pas été établie en cas de gestation ou de lactation.
Gestation:
L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable. Les études de laboratoire sur les souris et les lapins n’ont pas mis en évidence d’effets tératogènes. Une réduction de la fertilité a été observée chez les souris à partir de 5,6 mg/kg par jour.
Lactation:
L’utilisation n’est pas recommandée pendant la lactation. Chez les souris, une réduction du poids corporel et des taux de survie de la descendance ont été attribuées à l’inhibition pharmacologique de la sécrétion de prolactine, entraînant une chute de lactation.
3.8 Interactions médicamenteuses et autres formes d'interactions
Utiliser avec précaution en cas d’administration concomitante d’autres médicaments vétérinaires connus pour affecter la liaison aux protéines plasmatiques.
Ne pas administrer en même temps que des antagonistes de la dopamine, tels que les neuroleptiques (phénothiazines – par exemple, l’acépromazine), la dompéridone ou le métoclopramide, car ces molécules peuvent réduire l’efficacité du pergolide.
3.9 Voies d'administration et posologie
Voie orale, une fois par jour.
Pour faciliter l’administration, la dose journalière requise peut être dissoute dans un peu d’eau et/ou mélangée avec de la mélasse ou un autre produit sucré. Dans ce cas, les comprimés dissous doivent être administrés avec une seringue. La quantité totale doit être administrée immédiatement. Les comprimés ne doivent pas être écrasés voir rubrique 3.5.
Dose initiale
La dose initiale est d’environ 2 µg de pergolide par kg de poids vif (fourchette posologique: 1,3 à 2,5 µg/kg; voir le tableau ci-dessous). La dose d’entretien devra ensuite être ajustée en fonction de la réponse individuelle, telle que déterminée par le suivi (voir ci-dessous), pour parvenir à une dose d’entretien moyenne de 2 µg de pergolide par kg de poids vif, avec une fourchette posologique de 0,6 à 10 µg de pergolide par kg de poids vif.
Les doses initiales recommandées sont les suivantes :
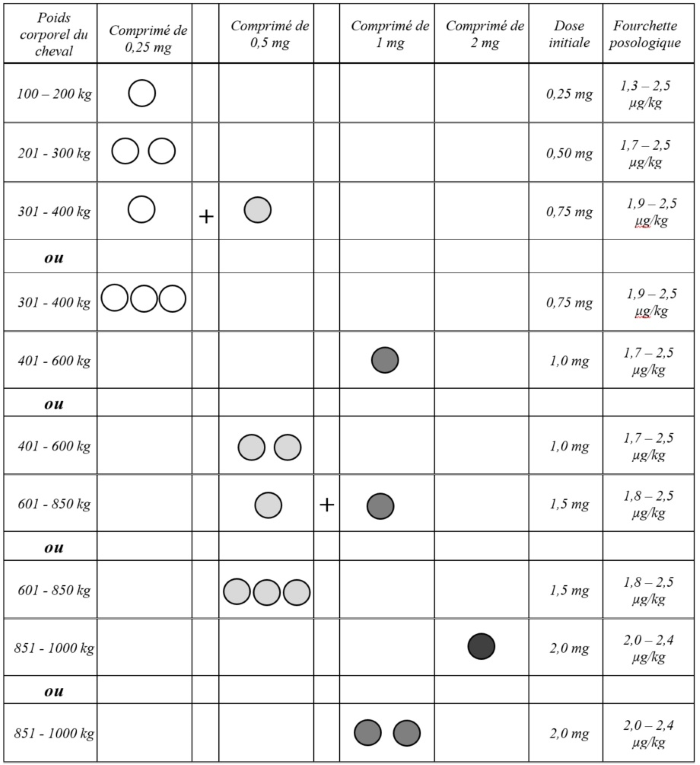
Dose d’entretien
Un traitement à vie est à envisager pour cette maladie.
La plupart des chevaux répondent au traitement et sont stabilisés à la dose moyenne de 2 µg de pergolide par kg de poids vif. L’amélioration clinique avec le pergolide est attendue en 6 à 12 semaines. Une réponse clinique peut survenir chez certains chevaux à des doses inférieures ou différentes ; c’est pourquoi il est recommandé d’ajuster la posologie individuellement jusqu’à la plus petite dose efficace, en se basant sur la réponse au traitement, évaluée d’après l’efficacité ou les signes d’intolérance. Certains chevaux pourront nécessiter des doses allant jusqu’à 10 µg de pergolide par kg de poids vif et par jour. Dans ces situations rares, il est conseillé de mettre en place un suivi plus poussé.
Après le diagnostic initial, répéter les tests endocriniens pour ajuster la posologie et surveiller le traitement à intervalles de 4 à 6 semaines jusqu’à stabilisation ou amélioration des signes cliniques et/ou réalisation de tests diagnostiques.
Si les signes cliniques ou les tests diagnostiques ne se sont pas améliorés au terme des premières 4 à 6 semaines, la dose totale journalière peut être augmentée de 0,25–0,50 mg. Si les signes cliniques se sont améliorés mais pas encore normalisés, le vétérinaire peut décider d’ajuster ou non la dose, en considérant la réponse/tolérance de l’animal à cette dose.
Au cas où les signes cliniques ne sont pas contrôlés de façon adéquate (évaluation clinique et/ou tests diagnostiques), il est recommandé d’augmenter la dose totale journalière par paliers de 0,25–0,5 mg (si le médicament est toléré à cette dose) toutes les 4 à 6 semaines jusqu’à stabilisation. En cas de signes d’intolérance, le traitement devra être suspendu durant 2 à 3 jours et réinstauré à la moitié de la dose précédente. La dose totale journalière pourra alors être réaugmentée jusqu’à l’effet clinique souhaité par paliers de 0,25–0,5 mg toutes les 2 à 4 semaines. En cas d’oubli d’une dose, la dose suivante devra être administrée normalement suivant la prescription.
Après stabilisation, une évaluation clinique régulière et des tests diagnostiques devront être effectués tous les 6 mois de façon à surveiller le traitement et la dose. S’il n’y a pas de réponse apparente au traitement, le diagnostic devra être réévalué.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Aucune information disponible.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Ne pas utiliser chez les chevaux destinés à la consommation humaine.
Les chevaux traités ne peuvent jamais être abattus à des fins de consommation humaine.
Le cheval doit avoir été déclaré exclu de la consommation humaine sur son livret d’identification, conformément aux dispositions réglementaires nationales.
Ne pas utiliser chez les animaux producteurs de lait destiné à la consommation humaine.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QN04BC02
4.2 Propriétés pharmacodynamiques
Le pergolide est un dérivé synthétique de l’ergot de seigle; c’est un agoniste des récepteurs de la dopamine, puissant et à longue durée d’action. Les études de pharmacologie in vitro et in vivo ont démontré que le pergolide agit comme un agoniste dopaminergique sélectif avec peu ou pas d’effet sur les voies noradrénergiques, adrénergiques ou sérotoninergiques aux doses thérapeutiques. Comme les autres agonistes dopaminergiques, le pergolide inhibe la sécrétion de prolactine. Chez les chevaux atteints de dysfonctionnement du lobe intermédiaire de l’hypophyse (PPID), le pergolide exerce son effet thérapeutique par stimulation des récepteurs de la dopamine. De plus, chez les chevaux atteints de PPID, il a été démontré que le pergolide diminue les taux plasmatiques d’ACTH, de MSH et des autres peptides précurseurs des hormones polypeptidiques (pro-opiomélanocortine).
4.3 Propriétés pharmacocinétiques
Des données pharmacocinétiques sont disponibles aux doses orales de 2, 4 et 10 μg de pergolide par kg de poids vif chez le cheval. Il a été démontré que le pergolide était rapidement absorbé, avec un délai d’obtention de la concentration maximale court.
Les concentrations maximales (Cmax) à la dose de 10 μg/kg ont été faibles et variables, avec une moyenne d’environ 4 ng/mL et une demi-vie moyenne d’élimination terminale (T½) d’environ 6 heures. Le délai médian d’obtention de la concentration maximale (Tmax) a été d’environ 0,4 heure et l’aire sous la courbe (ASC) d’environ 14 ng × h/mL.
Avec une méthode analytique plus sensible, les concentrations plasmatiques observées à la dose de 2 μg de pergolide/kg ont été très basses et variables, avec un pic de concentration compris entre 0,138 et 0,551 ng/mL. Les concentrations maximales ont été observées à 1,25 +/- 0,5 heure (Tmax). Les concentrations plasmatiques, chez la plupart des chevaux, n’étaient quantifiables que pendant les 6 heures suivant l’administration. Cependant, un cheval a présenté des concentrations quantifiables pendant 24 heures. Les demi-vies d’élimination terminale n’ont pas été calculées, car les concentrations plasmatiques en fonction du temps n’ont pas pu être déterminées en totalité pour la plupart des chevaux.
Les concentrations maximales (Cmax) après l’administration d’une dose de 4 µg/kg ont été faibles et variables, comprises dans une fourchette de 0,4 à 4,2 ng/mL, avec une moyenne de 1,8 ng/mL et une demi-vie terminale moyenne (T½) d’environ 6 heures. Le délai médian avant l’obtention des concentrations maximales (Tmax) a été d’environ 0,6 heure et l’ASCt s’élevait à environ 3,4 ng × h/mL.
Le mésilate de pergolide est associé approximativement à 90 % aux protéines plasmatiques chez les humains et les animaux de laboratoire. Le médicament vétérinaire est éliminé par voie rénale.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 30 mois.
5.3 Précautions particulières de conservation
À conserver à une température ne dépassant pas 30 °C.
À conserver dans l’emballage d’origine, de façon à le protéger de la lumière.
5.4 Nature et composition du conditionnement primaire
Plaquettes en PVC/PE/PVDC-aluminium, contenant 10 comprimés.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
ALFASAN NEDERLAND B.V.
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/4113894 4/2025
Boîte de 1 plaquette de 10 comprimés pelliculés
Boîte de 3 plaquettes de 10 comprimés pelliculés
Boîte de 6 plaquettes de 10 comprimés pelliculés
Boîte de 9 plaquettes de 10 comprimés pelliculés
Boîte de 10 plaquettes de 10 comprimés pelliculés
Boîte de 12 plaquettes de 10 comprimés pelliculés
Boîte de 16 plaquettes de 10 comprimés pelliculés
Boîte de 24 plaquettes de 10 comprimés pelliculés
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
03/12/2025
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
03/12/2025
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).