PIMOTAB 5 MG COMPRIMES A CROQUER POUR CHIENS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé à croquer contient : |
|
|
|
Substance active : |
|
Pimobendane………………………………………….. | 5 mg |
|
|
Excipients : |
|
Composition qualitative en excipients et autres composants |
Acide citrique |
Povidone K25 |
Lactose monohydraté |
Cellulose microcristalline |
Croscarmellose sodique |
Arôme poulet |
Levure déshydratée |
Silice colloïdale hydratée |
Stéarate de magnésium |
Comprimé marron clair avec des taches marron, rond et convexe, avec une barre de sécabilité sur une face en forme de croix.
Les comprimés peuvent être divisés en deux ou quatre parties égales.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens.
3.2 Indications d'utilisation pour chaque espèce cible
Traitement de l'insuffisance cardiaque congestive due à une cardiomyopathie dilatée ou à une insuffisance valvulaire (régurgitation valvulaire mitrale et/ou tricuspide).
(Voir aussi rubrique « 3.9 - Voies d'administration et posologie »).
3.3 Contre-indications
Ne pas utiliser le pimobendane en cas de cardiomyopathies hypertrophiques ou de maladies pour lesquelles l'amélioration du débit cardiaque n'est pas possible pour des raisons fonctionnelles ou anatomiques (par exemple, une sténose aortique).
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
3.4 Mises en garde particulières
Aucune.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
La glycémie doit être contrôlée régulièrement durant le traitement des chiens souffrant de diabète sucré.
Le pimobendane étant principalement métabolisé via le foie, il ne doit pas être utilisé chez les chiens présentant un dysfonctionnement hépatique sévère.
La surveillance de la fonction et de la morphologie cardiaques est recommandée chez les animaux traités avec le pimobendane (voir aussi rubrique « 3.6 - Effets indésirables »).
Les comprimés sont aromatisés. Conserver les comprimés hors de portée des animaux, afin d'éviter toute ingestion accidentelle.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le médicament vétérinaire peut entraîner une tachycardie, une hypotension orthostatique, une rougeur de la face et des maux de tête.
Pour éviter une ingestion accidentelle, en particulier par un enfant, les fractions de comprimés inutilisés doivent être réinsérés dans l’alvéole ouverte de la plaquette, replacés dans la boîte en carton et soigneusement gardés éloignés des enfants.
Les comprimés partiellement utilisés doivent être utilisés au moment de l’administration suivante.
En cas d'ingestion accidentelle, consultez immédiatement un médecin et montrez-lui la notice ou l'étiquette.
Se laver les mains après utilisation.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens :
Rare (1 à 10 animaux / 10 000 animaux traités) : | Vomissements1, diarrhée2 Anorexie2, léthargie2 Augmentation du rythme cardiaque1,3, accroissement de la régurgitation mitrale4 |
Très rare ( | Pétéchies sur les muqueuses5, hémorragies5 (sous-cutanées) |
1 Ces effets sont dose-dépendants et peuvent être évités en réduisant la dose administrée.
2 Transitoires.
3 Due à un léger effet chronotrope positif.
4 Observé durant le traitement de longue durée avec du pimobendane, chez des chiens souffrant de maladie valvulaire mitrale.
5 La relation de causalité avec le pimobendane n’a pas été clairement établie ; ces signes disparaissent à l’arrêt du traitement.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation :
Les études de laboratoire menées chez des rats et des lapins n'ont pas mis en évidence d'effets tératogènes ou fœtotoxiques. Cependant, ces études ont mis en évidence des effets maternotoxiques et embryotoxiques à fortes doses.
L'innocuité du médicament vétérinaire n'a pas été évaluée chez les chiennes gestantes. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
Lactation :
Les études de laboratoire menées chez des rats ont aussi montré que le pimobendane est excrété dans le lait.
L'innocuité du médicament vétérinaire n'a pas été évaluée chez les chiennes allaitantes. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
3.8 Interactions médicamenteuses et autres formes d'interactions
Aucune interaction entre la strophantine, glycoside cardiaque, et le pimobendane n'a été observée dans les études pharmacologiques. L'accroissement de la contractilité cardiaque induite par le pimobendane est atténué par les inhibiteurs calciques et par les bêtabloquants.
3.9 Voies d'administration et posologie
Voie orale.
Ne pas dépasser la dose recommandée.
Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible.
La dose doit être administrée oralement et à une dose comprise entre 0,2 à 0,6 mg de pimobendane/kg de poids corporel par jour, divisée en deux prises quotidiennes. La dose quotidienne conseillée est de 0,5 mg de pimobendane/kg de poids corporel, divisée en deux prises quotidiennes (0,25 mg/kg de poids corporel par prise). Chaque prise doit être donnée approximativement 1 heure avant la prise alimentaire.
Ceci correspond à :
Un comprimé à croquer de 5 mg le matin et un comprimé à croquer de 5 mg le soir pour un poids corporel de 20 kg.
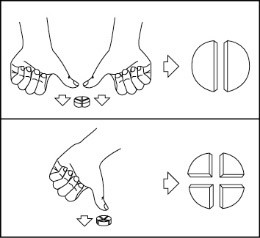
Les comprimés à croquer peuvent être divisés en 2 ou 4 parties égales, pour l'administration d'une dose correcte, en fonction du poids corporel.
Placez le comprimé sur une surface plane, avec la face gravée vers le haut et la face convexe (arrondie) vers la surface.
Pour diviser en 2 fractions égales :
Appuyez vers le bas, avec vos pouces, sur les 2 bords opposés du comprimé.
Pour diviser en 4 fractions égales :
Appuyez vers le bas, avec un pouce, au centre du comprimé.
Le médicament vétérinaire peut être associé à un diurétique, comme le furosémide par exemple.
En cas d’insuffisance cardiaque congestive, un traitement à vie est recommandé. La dose d'entretien doit être ajustée individuellement en fonction de la gravité de la maladie.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
En cas de surdosage, un effet chronotrope positif, des vomissements, une apathie, une ataxie, des murmures cardiaques ou une hypotension peuvent apparaître. Il est alors nécessaire de réduire la dose et d'instaurer un traitement symptomatique approprié.
Lors d'exposition prolongée (6 mois) chez le chien Beagle sain à trois à cinq fois la dose recommandée, un épaississement de la valvule mitrale et une hypertrophie ventriculaire gauche ont été observés chez certains chiens. Ces changements sont d'origine pharmacodynamique.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QC01CE90.
4.2 Propriétés pharmacodynamiques
En cas d'insuffisance valvulaire symptomatique, lors d'utilisation en association avec le furosémide, le médicament vétérinaire a démontré une amélioration de la qualité de vie et un allongement de la durée de vie chez les chiens traités.
Dans un nombre limité de cas de cardiomyopathies dilatées symptomatiques, lors d'utilisation en association avec le furosémide, l'énalapril et la digoxine, le médicament vétérinaire a démontré une amélioration de la qualité de vie et un allongement de la durée de vie chez les chiens traités.
Le pimobendane, un dérivé du benzimidazole-pyridazinone, a une action inotrope positive et possède de puissantes propriétés vasodilatatrices.
L'effet inotrope positif du pimobendane est obtenu par deux mécanismes d'action : un accroissement de la sensibilité au calcium des myofilaments cardiaques et une inhibition de la phosphodiestérase III. Ainsi l'effet inotrope positif n'est déclenché ni par une action similaire à celle des glycosides cardiaques ni par un mécanisme sympathomimétique.
L'effet vasodilatateur provient de l'inhibition de la phosphodiestérase III.
4.3 Propriétés pharmacocinétiques
Après administration orale de ce médicament vétérinaire, la biodisponibilité absolue de la substance active est de 60 - 63%. Cette biodisponibilité est considérablement réduite quand le pimobendane est administré avec de la nourriture ou peu de temps après.
Après administration orale d’une dose unique de 0,2 – 0,4 mg/kg de pimobendane aux chiens à jeun, les concentrations plasmatiques ont augmenté rapidement.
La concentration maximale (Cmax) de ~ 24 ng/mL est atteinte en 0,75 heure médian (Tmax variait de 0,25 à 2,5 heures).
Le volume de distribution est de 2,6 L/kg, indiquant que le pimobendane est rapidement distribué dans les tissus. Le taux moyen de liaison aux protéines plasmatiques est de 93 %.
Le composé est déméthylé par oxydation en son principal métabolite actif (UD-CG 212). Les étapes métaboliques suivantes sont des conjugués de phase II du UD-CG 212, tels que glucuronides et sulfates.
Le temps de demi-vie d'élimination plasmatique du pimobendane est d’environ 1 heure. La dose est presque totalement excrétée par voie fécale.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 5 ans
Durée de conservation des comprimés divisés après première ouverture du conditionnement primaire : 3 jours
5.3 Précautions particulières de conservation
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
5.4 Nature et composition du conditionnement primaire
Plaquette thermoformée Aluminium-OPA/Aluminium/PVC de 10 comprimés quadrisécables.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
CP-PHARMA HANDELSGESELLSCHAFT MBH
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/8560607 8/2020
Boîte de 3 plaquettes de 10 comprimés quadrisécables
Boîte de 5 plaquettes de 10 comprimés quadrisécables
Boîte de 10 plaquettes de 10 comprimés quadrisécables
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
17/12/2020
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
12/12/2025
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).