PREDNICORTONE 20 MG COMPRIMES POUR CHIENS ET CHATS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un comprimé contient :
Substance active :
Prednisolone 20 mg
Excipients :
Composition qualitative en excipients et autres composants |
Levure (déshydratée) |
Arôme poulet |
Lactose monohydraté |
Cellulose en poudre |
Carboxyméthylamidon sodique (type A) |
Stéarate de magnésium |
Comprimé marron clair tacheté de brun, rond et convexe, aromatisé, avec une barre de sécabilité en croix sur une face.
Les comprimés peuvent être divisés en 2 ou 4 parties égales.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens et chats.
3.2 Indications d'utilisation pour chaque espèce cible
Traitement symptomatique ou traitement d’appoint des maladies inflammatoires et des maladies d’origine immunologique chez les chiens et les chats.
3.3 Contre-indications
Ne pas utiliser chez les animaux souffrant d’infections virales ou mycosiques non contrôlées par un traitement approprié.
Ne pas utiliser chez les animaux souffrant d'un diabète sucré ou d’hypercorticisme. Ne pas utiliser chez les animaux atteints d’ostéoporose.
Ne pas utiliser chez les animaux souffrant d’une insuffisance cardiaque ou rénale.
Ne pas utiliser chez les animaux souffrant d’ulcères cornéens.
Ne pas utiliser chez les animaux atteints d’ulcères gastro-intestinaux.
Ne pas utiliser chez les animaux présentant des brûlures.
Ne pas utiliser en concomitance avec un vaccin vivant atténué.
Ne pas utiliser en cas de glaucome.
Ne pas utiliser au cours de la gestation (voir la rubrique 3.7).
Ne pas utiliser en cas d’hypersensibilité connue à la substance active, aux corticostéroïdes ou à l’un des excipients.
Voir également la rubrique 3.8.
3.4 Mises en garde particulières
L’administration de corticoïdes vise à induire une amélioration des signes cliniques plutôt qu’à obtenir une guérison. Le traitement doit être associé à un traitement de la maladie sous-jacente et/ou à des mesures de contrôle environnemental.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Si une infection bactérienne est présente, le médicament vétérinaire doit être utilisé en association avec un traitement antibactérien adapté.
En raison des propriétés pharmacologiques de la prednisolone, le médicament vétérinaire doit être utilisé avec une précaution particulière chez les animaux dont le système immunitaire est affaibli.
Les corticoïdes, tels que la prednisolone, exacerbent le catabolisme protéique. Par conséquent, le médicament vétérinaire doit être administré avec précaution chez les animaux âgés ou dénutris.
Aux doses actives d’un point de vue pharmacologique, le produit peut entraîner une atrophie de la corticosurrénale, engendrant une insuffisance surrénale. Cet effet peut être particulièrement manifeste après l’arrêt du traitement par corticostéroïde. L’insuffisance surrénale peut être limitée au maximum en instituant le traitement un jour sur deux, si cela est réalisable. La réduction de la posologie et l’arrêt du traitement doivent être progressifs afin d’éviter de précipiter une insuffisance surrénale (voir la rubrique 3.9).
Les corticoïdes, tels que la prednisolone, doivent être utilisés avec prudence chez les animaux souffrant d’hypertension, d’épilepsie, chez les animaux avec un historique de myopathie stéroïdienne, chez les animaux immunodéprimés et chez les jeunes animaux étant donné que les corticostéroïdes peuvent induire un retard de croissance.
Les comprimés sont aromatisés. Afin d'éviter toute ingestion accidentelle, conserver les comprimés hors de portée des animaux.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
La prednisolone ou les autres corticostéroïdes peuvent provoquer des réactions d’hypersensibilité (allergie).
Les personnes présentant une hypersensibilité connue à la prednisolone, à d’autres corticostéroïdes ou à l’un des excipients doivent éviter tout contact avec le médicament vétérinaire.
Afin d’éviter toute ingestion accidentelle, en particulier par un enfant, les fractions de comprimés non utilisées doivent être replacées dans l’alvéole ouverte de la plaquette et remises dans la boîte.
En cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Les corticostéroïdes pouvant provoquer des malformations fœtales, il est recommandé aux femmes enceintes d’éviter tout contact avec le médicament vétérinaire.
Se laver immédiatement et soigneusement les mains après avoir manipulé les comprimés.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens et chats :
Très fréquent ( > 1 animal / 10 animaux traités) : | Suppression du cortisol1, augmentation des triglycérides2 |
Très rare ( < 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Excitation Pancréatite Syndrome de Cushing3, diabète sucré Hépatomégalie Augmentation du taux sérique de phosphatase alcaline (PAL)4, élévation des enzymes hépatiques, éosinopénie, neutrophilie5, lymphopénie, hypokaliémie6, thyroxine (T4) basse Faiblesse musculaire, perte de masse musculaire Polyurie7 Atrophie cutanée, calcinose cutanée Polyphagie7, polydispsie7 |
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) | Ulcères gastroduodénaux8 Diminution de l’aspartate transaminase (ASAT), diminution de la lactate déshydrogénase (LDH), hyperalbuminémie, tri-iodothyronine (T3) basse, augmentation de la concentration des hormones parathyroïdiennes (PTH) Inhibition de la croissance longitudinale des os, ostéoporose Retard de cicatrisation9, rétention hydro-sodée6, altération du métabolisme des lipides, prise de poids Immunosuppression10, affaiblissement de la résistance aux infections ou exacerbation d’infections existantes10 Insuffisance surrénale11, atrophie corticosurrénale11 |
1 liée à la dose, conséquence de la suppression de l’axe hypothalamo-hypophyso-surrénalien par les doses efficaces.
2 peut être liée à un éventuel hypercorticisme iatrogène (syndrome de Cushing).
3 iatrogène, impliquant une altération significative du métabolisme des lipides, glucides, protéines et minéraux.
4 pourrait être liée à une augmentation du volume du foie (hépatomégalie) associée à une élévation des enzymes hépatiques sériques.
5 augmentation des neutrophiles segmentés.
6 en cas d’utilisation à long terme.
7 après administration par voie systémique, en particulier dans les premiers temps du traitement.
8 peuvent être exacerbés par les stéroïdes chez les animaux recevant des anti-inflammatoires non stéroïdiens et les animaux présentant un traumatisme de la moelle épinière.
9 des plaies.
10 En présence d’infections virales, les corticostéroïdes peuvent aggraver ou accélérer l’évolution de la maladie.
11 peuvent apparaître après l’arrêt du traitement, ce qui peut rendre l’animal incapable de faire face de façon adéquate à des situations de stress. Il convient donc d’envisager des moyens de limiter au maximum les problèmes d’insuffisance surrénale après l’arrêt du traitement.
Les corticostéroïdes anti-inflammatoires, tels que la prednisolone, sont connus pour provoquer une grande diversité d’effets indésirables. Si les doses élevées sont généralement bien tolérées en administration unique, elles peuvent induire des effets indésirables sévères en cas d’utilisation à long terme. Par conséquent, lors d’une administration à moyen ou long terme, la posologie devra généralement être maintenue au niveau minimal requis pour contrôler les symptômes.
Voir également la rubrique 3.7.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation et lactation :
Ne pas utiliser durant la gestation.
Les études de laboratoire sur les animaux ont montré que l’administration du médicament en début de gestation pouvait provoquer des anomalies fœtales. Son administration à un stade plus tardif de la gestation peut entraîner un avortement ou une parturition prématurée. Voir la rubrique 3.3.
Les glucocorticoïdes sont excrétés dans le lait et peuvent conduire à un retard de croissance chez les jeunes animaux qui tètent leur mère.
L’utilisation au cours de la lactation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
3.8 Interactions médicamenteuses et autres formes d'interactions
La phénytoïne, les barbituriques, l’éphédrine et la rifampicine peuvent accélérer la clairance métabolique des corticostéroïdes, entraînant une réduction des concentrations sanguines et des effets physiologiques du médicament.
L’utilisation concomitante de ce médicament vétérinaire et d’anti-inflammatoires non stéroïdiens peut exacerber les ulcères gastroduodénaux. Dans la mesure où les corticostéroïdes peuvent réduire la réponse immunologique à la vaccination, la prednisolone ne doit pas être utilisée en même temps que des vaccins ni dans les deux semaines suivant une vaccination.
L’administration de prednisolone peut induire une hypokaliémie et donc augmenter le risque de toxicité des glucosides cardiotoniques. Le risque d’hypokaliémie peut être majoré si la prednisolone est administrée en association avec des diurétiques hypokaliémiants.
3.9 Voies d'administration et posologie
Voie orale.
La dose et la durée totale du traitement doivent être déterminées au cas par cas par le vétérinaire en fonction de la sévérité des symptômes. La plus faible dose efficace doit être utilisée.
Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible.
Dose initiale : 0,5 – 4 mg de prednisolone par kg de poids corporel par jour.
Traitement plus durable : lorsque, à l’issue d’une période d’administration quotidienne, l’effet recherché a été obtenu, la dose doit être réduite jusqu’à atteindre la plus faible dose efficace. La réduction de la dose doit être effectuée au moyen d’un traitement alterné un jour sur deux et/ou en divisant la dose par deux à intervalles de 5 à 7 jours jusqu’à atteindre la plus faible dose efficace.
Les chiens doivent être traités le matin et les chats le soir afin de tenir compte des différences de rythme circadien.
Les comprimés peuvent être divisés en 2 ou 4 parties égales pour obtenir l’exacte posologie nécessaire. Placez le comprimé sur une surface plate, avec la face portant la barre de sécabilité tournée vers le haut et la face convexe (arrondie) tournée vers le plan de travail.
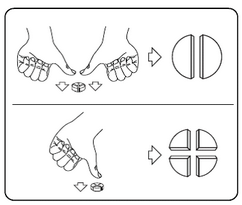
Moitiés : appuyez avec vos pouces des deux côtés du comprimé.
Quarts : appuyez avec votre pouce au centre du comprimé.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Le surdosage ne provoque pas d’autres effets indésirables que ceux mentionnés dans la rubrique 3.6. Il n’existe aucun antidote connu.
Les signes de surdosage doivent être traités de façon symptomatique.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QH02AB06.
4.2 Propriétés pharmacodynamiques
La prednisolone est un corticostéroïde semi-synthétique dérivé de l’hydrocortisone naturelle (cortisol). Cependant, ses effets sur le métabolisme des minéraux et du glucose sont (environ deux fois) plus faibles que ceux du cortisol. Cela permet de limiter au maximum les problèmes de rétention hydrique et d’hypertension.
La prednisolone exerce un effet de nature anti-inflammatoire. Lorsque la réaction inflammatoire est utile (par exemple, pour empêcher la prolifération de micro-organismes de se poursuivre), la suppression de ce mécanisme de défense est contre-productive. À l’inverse, lorsque la réponse inflammatoire est excessive et/ou nocive (p. ex., en réponse à un processus auto-immun ou allergique), la réponse inflammatoire de défense aggrave la situation et sa répression au moyen de corticostéroïdes peut avoir une grande importance thérapeutique.
- La formation de tissu de granulation est inhibée par l’effet de catabolisme protéique.
- L’inhibition de l’inflammation est également le résultat de l’effet stabilisateur de la prednisolone sur les membranes lysosomales.
- Les corticostéroïdes réduisent la formation d’exsudats inflammatoires et d’œdèmes locaux en stimulant la vasoconstriction et en diminuant la perméabilité des capillaires.
- Effet anti-allergique et immunosuppression : ces effets sont en partie liés à l’activité anti-inflammatoire du produit et sont principalement dirigés contre l’immunoréactivité cellulaire (lymphocytes T).
Étant donné que les effets thérapeutiques des corticostéroïdes administrés par voie systémique n’apparaissent qu’au bout de plusieurs heures, ces derniers sont moins adaptés au traitement des réactions anaphylactiques (aiguës) telles que le choc septique.
4.3 Propriétés pharmacocinétiques
Après administration orale, la prednisolone est bien absorbée dans le tube gastro-intestinal et distribuée dans tous les tissus, les fluides corporels et même le liquide céphalorachidien. La prednisolone se lie très largement aux protéines plasmatiques. Elle est métabolisée dans le foie et excrétée principalement par les reins.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
Durée de conservation des fractions de comprimés : 4 jours.
5.3 Précautions particulières de conservation
Les fractions de comprimé inutilisées doivent être réintroduites dans la plaquette entamée qui doit être remise dans la boîte.
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation en ce qui concerne la température.
5.4 Nature et composition du conditionnement primaire
Plaquette PVDC/PE/PVC-aluminium
Boîte en carton contenant 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 25 ou 50 plaquettes de 10 comprimés.
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
DECHRA REGULATORY B.V.
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/1747250 6/2015
Boîte en carton de 1 plaquette de 10 comprimés
Boîte en carton de 2 plaquettes de 10 comprimés
Boîte en carton de 3 plaquettes de 10 comprimés
Boîte en carton de 4 plaquettes de 10 comprimés
Boîte en carton de 5 plaquettes de 10 comprimés
Boîte en carton de 6 plaquettes de 10 comprimés
Boîte en carton de 7 plaquettes de 10 comprimés
Boîte en carton de 8 plaquettes de 10 comprimés
Boîte en carton de 9 plaquettes de 10 comprimés
Boîte en carton de 10 plaquettes de 10 comprimés
Boîte en carton de 25 plaquettes de 10 comprimés
Boîte en carton de 50 plaquettes de 10 comprimés
Boîte en carton de 15 plaquettes de 10 comprimés
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
16/06/2015
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
04/04/2025
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).