SPIZOBACTIN 3 000 000 UI / 500 MG COMPRIMES A CROQUER POUR CHIENS
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé contient : |
|
|
|
Substances actives : |
|
Spiramycine …………………………………………… | 3 000 000 UI |
Métronidazole …………………………………………. | 500 mg |
|
|
Excipients : |
|
Composition qualitative en excipients et autres composants |
Amidon prégélatinisé |
Cellulose microcristalline |
Lactose monohydraté |
Hydroxypropylcellulose |
Levure déshydratée |
Arôme poulet |
Silice colloïdale anhydre |
Stéarate de magnésium |
Comprimé à croquer brun clair moucheté de brun, rond et convexe, avec une barre de sécabilité cruciforme sur une face.
Les comprimés peuvent être divisés en 2 ou 4 parts égales.
3. INFORMATIONS CLINIQUES
3.1 Espèces cibles
Chiens.
3.2 Indications d'utilisation pour chaque espèce cible
Pour le traitement d’appoint d’une thérapie parodontale mécanique ou chirurgicale, dans le traitement des infections multibactériennes parodontales et affectant la sphère (péri) buccale - par exemple stomatite, gingivite, glossite, parodontite, amygdalite, fistule dentaire et autres plaies fistulaires de la cavité buccale, chéilite et sinusite - chez les chiens, causées par des microorganismes sensibles à la spiramycine /au métronidazole, tels que les bactéries Gram positif et les anaérobies (voir aussi rubriques « 3.4 - Mises en garde particulières » et « 3.5 - Précautions particulières d'emploi »).
3.3 Contre-indications
Ne pas utiliser en cas de troubles hépatiques.
Ne pas utiliser en cas d'hypersensibilité aux substances actives ou à l'un des excipients.
3.4 Mises en garde particulières
Dans de nombreux cas de maladie de l’endodonte / du parodonte, le traitement primaire est non médical et ne nécessite pas de traitement antimicrobien.
Le traitement antimicrobien de la maladie parodontale doit être accompagné ou précédé d'un traitement de l’endodonte et / ou d'un nettoyage de la dentition par un professionnel, surtout si la maladie est à un stade avancé. Les propriétaires de chiens sont encouragés à brosser régulièrement les dents de leur chien pour enlever la plaque, afin d’éviter ou de contrôler la maladie parodontale.
3.5 Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
L’association de spiramycine et de métronidazole ne doit pas être utilisée empiriquement comme traitement initial.
Dans la mesure du possible, le métronidazole et la spiramycine ne doivent être utilisés que sur la base de tests de sensibilité.
Le médicament vétérinaire doit être utilisé conformément aux politiques officielles, nationales et régionales concernant l’antibiothérapie.
La limitation de la durée du traitement est nécessaire car des dommages aux cellules germinales ne peuvent pas être exclus avec l'utilisation du métronidazole et, dans les études à long terme à fortes doses, une augmentation de certaines tumeurs a été observée chez les rongeurs.
Les comprimés à croquer sont aromatisés. Afin d’éviter toute ingestion accidentelle, conserver les comprimés hors de portée des animaux.
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le métronidazole a montré des propriétés mutagènes et génotoxiques chez les animaux de laboratoire ainsi que chez les humains. Le métronidazole est un agent cancérogène confirmé chez les animaux de laboratoire et a des effets cancérogènes possibles chez l'homme. Cependant, il existe des preuves insuffisantes chez l'homme concernant la cancérogénicité du métronidazole.
Le métronidazole peut être nocif pour le fœtus.
Les femmes enceintes doivent être prudentes lorsqu'elles manipulent ce médicament vétérinaire.
La spiramycine et le métronidazole peuvent, dans de rares cas, induire des réactions d'hypersensibilité, par exemple une dermatite de contact.
Le contact direct avec la peau ou les muqueuses de l'utilisateur doit être évité en raison du risque de sensibilisation. Les personnes présentant une hypersensibilité connue aux substances actives ou à l'un des excipients doivent éviter tout contact avec le médicament vétérinaire.
Un équipement de protection individuelle consistant en des gants imperméables doit être porté lors de la manipulation du médicament vétérinaire afin d'éviter tout contact cutané avec le médicament vétérinaire et tout contact main-bouche.
Le métronidazole peut provoquer des effets indésirables (effets neurologiques) en cas d'ingestion par un enfant.
Pour éviter une ingestion accidentelle, en particulier par un enfant, les morceaux de comprimés inutilisés doivent être réinsérés dans les espaces libres de la plaquette, et remis dans la boîte en carton. En cas d'ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Lavez-vous soigneusement les mains après avoir manipulé les comprimés.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
3.6 Effets indésirables
Chiens :
Rare (1 à 10 animaux / 10 000 animaux traités) : | Vomissements Hypersensibilité a |
Très rare (< 1 animal / 10 000 animaux traités, y compris les cas isolés) : | Hématurie Affection de l’appareil reproducteur chez les mâles b |
a En cas de réactions d’hypersensibilité, le traitement doit être arrêté.
b Trouble de la spermatogenèse
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
3.7 Utilisation en cas de gestation, de lactation ou de ponte
Gestation et lactation :
La spiramycine ne s’est pas avérée tératogène ou embryo- ou fœtotoxique. Les études de laboratoire sur les animaux ont montré des résultats peu cohérents en ce qui concerne les effets tératogènes / embryotoxiques du métronidazole. Le métronidazole et la spiramycine sont excrétés dans le lait. Utilisation non recommandée durant la gestation et la lactation.
3.8 Interactions médicamenteuses et autres formes d'interactions
Ne pas utiliser de manière concomitante avec des antibiotiques bactéricides.
Les macrolides, comme par exemple la spiramycine, agissent de façon antagoniste par rapport aux pénicillines et aux céphalosporines.
Le médicament vétérinaire ne doit pas être utilisé simultanément avec d'autres antibiotiques du groupe des macrolides.
Le métronidazole peut avoir un effet inhibiteur sur la dégradation d'autres médicaments dans le foie, tels que la phénytoïne, la cyclosporine et la warfarine.
Le phénobarbital peut augmenter le métabolisme hépatique du métronidazole, ce qui entraîne une diminution de la concentration sérique de métronidazole.
3.9 Voies d'administration et posologie
Voie orale.
75 000 UI de spiramycine + 12,5 mg de métronidazole par kg de poids corporel, dans des cas plus graves 100 000 UI de spiramycine + 16,7 mg de métronidazole par kg de poids corporel, administrés quotidiennement pendant 6 à 10 jours selon la gravité de la maladie.
Dans les cas graves, on peut commencer par la dose plus élevée et revenir en cours de traitement à la dose plus faible.
La dose quotidienne peut être administrée une fois par jour ou divisée en doses égales pour une administration deux fois par jour.
Le traitement doit toujours être poursuivi pendant 1-2 jours après la disparition des symptômes afin de prévenir les rechutes. Les comprimés doivent être administrés soit profondément dans la bouche (sur la base de la langue), soit administrés avec une petite quantité de nourriture contenant le comprimé, afin d'assurer la consommation totale du comprimé.
Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible. Le tableau suivant est conçu comme un guide pour administrer le médicament vétérinaire approximativement à la posologie standard de 75 000 UI de spiramycine + 12,5 mg de métronidazole par kg de poids corporel.
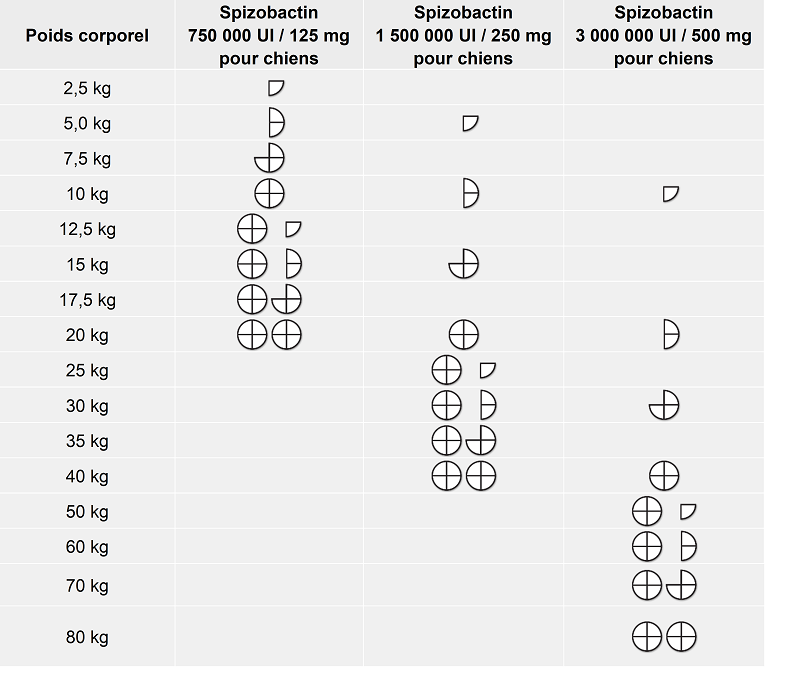

Les comprimés peuvent être divisés en 2 ou 4 parts égales pour assurer un dosage précis. Placez le comprimé sur une surface plane, avec son côté rainuré vers le haut et le côté convexe (arrondi) face à la surface.
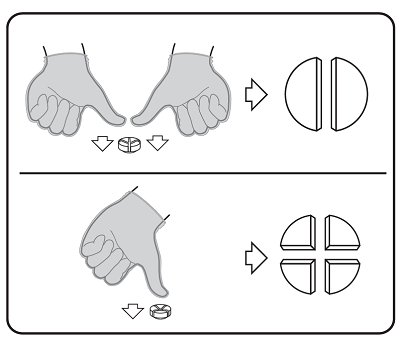
2 parts égales : appuyez vers le bas avec vos pouces sur des deux côtés du comprimé.
4 parts égales : appuyez vers le bas avec votre pouce au milieu du comprimé.
3.10 Symptômes de surdosage (et, le cas échéant, conduite d'urgence et antidotes)
Si des signes neurologiques se produisent, le traitement doit être interrompu et l'animal doit être traité de manière symptomatique.
3.11 Restrictions d'utilisation spécifiques et conditions particulières d'emploi, y compris les restrictions liées à l'utilisation de médicaments vétérinaires antimicrobiens et antiparasitaires en vue de réduire le risque de développement de résistance
Sans objet.
3.12 Temps d'attente
Sans objet.
4. INFORMATIONS PHARMACOLOGIQUES
4.1 Code ATCvet
QJ01RA04.
4.2 Propriétés pharmacodynamiques
La spiramycine est un antibiotique du groupe des macrolides. Elle agit de façon nettement bactériostatique, par inhibition de la synthèse des protéines (interférant avec la réaction de traduction au niveau des ribosomes). Son spectre d'activité comprend principalement les bactéries Gram positif. Trois mécanismes différents sont à l’origine de la plupart des résistances bactériennes à l'action des macrolides : (1) méthylation de l'ARNr ; (2) efflux actif, et (3) inactivation enzymatique. Les deux premiers mécanismes sont les plus fréquents et les gènes codant ces mécanismes se situent souvent sur des éléments mobiles. La méthylation de l'ARNr, codée par les gènes ERM (erythromycine resistant methylase), entraîne une résistance croisée avec les macrolides, les lincosamides et la streptogramine B (résistance MLSB).
Le métronidazole est un dérivé imidazolique et agit contre les représentants des protozoaires (flagellés et amibes) et contre les anaérobies Gram positif et Gram négatif.
L'association de la spiramycine et du métronidazole élargit le spectre, en raison du profil antibactérien complémentaire des deux médicaments. Des effets synergiques ont été démontrés sur certains agents pathogènes dans des études in vitro et dans des infections expérimentales d'animaux de laboratoire.
4.3 Propriétés pharmacocinétiques
Après administration orale, des concentrations plasmatiques maximales de spiramycine-I (composant principal de la spiramycine) de 4,4 μg/mL sont obtenues dans un délai de 1,3 heure. La spiramycine atteint rapidement de fortes concentrations tissulaires qui sont 10 à 15 fois plus élevées que dans le plasma. Les concentrations dans les muqueuses et la salive sont particulièrement élevées. Après une seule dose orale de spiramycine, des concentrations restent présentes pendant environ 30 à 40 heures.
La spiramycine est éliminée par la bile chez le chien. La demi-vie terminale est d'environ 8,6 heures.
Après administration orale, des concentrations plasmatiques maximales de métronidazole de 18 μg/mL sont obtenues dans un délai de 1,4 heure. Après ingestion orale, le métronidazole diffuse rapidement et complètement dans tous les tissus du corps. Après 24 heures, des concentrations sanguines supérieures à 0,5 μg/mL sont encore détectables chez la plupart des chiens. L'excrétion se fait via l'urine. La demi-vie terminale est d'environ 5,3 heures.
Propriétés environnementales
5. DONNÉES PHARMACEUTIQUES
5.1 Incompatibilités majeures
Sans objet.
5.2 Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 18 mois.
Durée de conservation des fractions de comprimé : 3 jours.
5.3 Précautions particulières de conservation
À conserver à une température ne dépassant pas 30°C.
5.4 Nature et composition du conditionnement primaire
Plaquette thermoformée aluminium - PVC/PE/PVDC
5.5 Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
6. NOM DU TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ
LE VET. BEHEER B.V.
7. NUMÉRO(S) D'AUTORISATION DE MISE SUR LE MARCHÉ
FR/V/0556981 8/2017
Boîte de 1 plaquette de 10 comprimés quadrisécables
Boîte de 2 plaquettes de 10 comprimés quadrisécables
Boîte de 3 plaquettes de 10 comprimés quadrisécables
Boîte de 10 plaquettes de 10 comprimés quadrisécables
Boîte de 10 boîtes de 1 plaquette de 10 comprimés quadrisécables
Toutes les présentations peuvent ne pas être commercialisées.
8. DATE DE PREMIÈRE AUTORISATION
28/08/2017
9. DATE DE LA DERNIÈRE MISE À JOUR DU RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
13/02/2026
MARCHES LIMITES
CIRCONSTANCES EXCEPTIONNELLES
10. CLASSIFICATION DES MEDICAMENTS VETERINAIRES
Médicament vétérinaire soumis à ordonnance.
Des informations détaillées sur ce médicament vétérinaire sont disponibles dans la base de données de l’Union sur les médicaments (https://medicines.health.europa.eu/veterinary).